Kyánhydrín
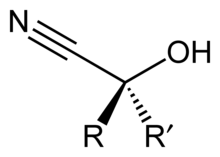
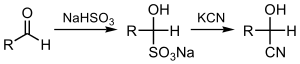
Kyánhydrín je funkčná skupina, v ktorej sú kyano a hydroxylová skupina naviazané na rovnaký atóm uhlíka.[1][2] Všeobecný vzorec je R2C(OH)CN, kde R je H, alkyl alebo aryl. Kyánhydríny sú priemyselne dôležité prekurzory karboxylových kyselín a niektorých aminokyselín. Kyánhydríny môžu byť vytvorené kyánhydrínovou syntézou, ktorá zahŕňa reakciu ketónu alebo aldehydu s kyanovodíkom (HCN) v prítomnosti nadbytočného množstva kyanidu sodného (NaCN) ako katalyzátora:[2][3]
- RR'C=O + HCN → RR'C(OH)CN
V tejto reakcii napadá nukleofilný ión CN- elektrofilný karbonylový uhlík v ketóne či aldehyde a potom nasleduje protonácia pomocou HCN, čím sa regeneruje kyanidový anión. Kyánhydríny sa tiež pripravujú vytesnením siričitanu kyanidovými soľami:[4]
Kyánhydríny sú medziprodukty v Streckerovej syntéze aminokyselín. Vo vodných roztokoch kyselín hydrolyzujú na α-hydroxykyseliny.
Metódy prípravy[upraviť | upraviť zdroj]
Kyánhydríny sa najskôr pripravovali pridaním HCN a katalyzátora (zásady alebo enzýmu) k zodpovedajúcemu karbonylu.[5] Zásada spôsobuje deprotonáciu málo reaktívneho kyanovodíku, HCN, čím vznikajú CN- ióny.[2] V laboratórnom merítku sa použitie (toxického) HCN vo veľkej miere neodporúča, z tohto dôvodu sa hľadajú iné menej nebezpečné kyanačné činidlá. In situ tvorbu HCN možno docieliť práve pomocou prekurzorov, ako je acetónkyánhydrín. Alternatívne, kyano-silylderiváty, ako je TMS-CN, umožňujú kyanáciu aj ochranu skupiny v jednom kroku bez potreby HCN.[6] Boli opísané podobné postupy založené na tvorbe esterov, fosforečnanov a uhličitanov.[7][8][9]

Príklady[upraviť | upraviť zdroj]
Acetónové kyánhydríny[upraviť | upraviť zdroj]
Acetónkyanohydrín, (CH3)2C(OH)CN, je kyánhydrín acetónu. Vzniká ako medziprodukt pri priemyselnej výrobe metylmetakrylátu.[10] V laboratóriu táto kvapalina slúži ako zdroj HCN, ktorý je inak veľmi prchavý. [11] Acetónkyánhydrín sa teda môže použiť na prípravu iných kyánhydrínov, na premenu HCN na Michaelove akceptory a na formyláciu arénov. Reakciou tohto kyánhydrínu s hydridom lítnym vzniká bezvodý kyanid lítny:
Iné kyánhydríny[upraviť | upraviť zdroj]
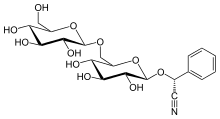
Mandelonitril so vzorcom C6H5CH(OH)CN sa v malých množstvách vyskytuje v kôstkach niektorých druhov ovocia.[4] Sú známe príbuzné kyanogénne glykozidy, ako je amygdalín.[3] Tieto glykozidy majú namiesto hydroxylovej skupiny glykozid.
Glykolonitril je organická zlúčenina so vzorcom HOCH2CN . Je to najjednoduchší kyánhydrín, odvodený od formaldehydu.[12]
-
glykolonitril
-
acetónkyanohydrín
-
mandelonitril
Referencie[upraviť | upraviť zdroj]
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "cyanohydrins". DOI:https://doi.org/10.1351/goldbook
- ↑ a b c kyánhydrínová syntéza. In: BÍNA, Jaroslav. Malá encyklopédia chémie. Bratislava : Obzor, 1981. S. 402.
- ↑ a b MOWRY, David T.. The Preparation of Nitriles.. Chemical Reviews, 1948-04-01, roč. 42, čís. 2, s. 189–283. Dostupné online [cit. 2022-09-19]. ISSN 0009-2665. DOI: 10.1021/cr60132a001. (po anglicky)
- ↑ a b Organic Syntheses Procedure [online]. www.orgsyn.org, [cit. 2022-09-19]. Dostupné online. (po anglicky)
- ↑ NORTH, Michael; USANOV, Dmitry L.; YOUNG, Carl. Lewis Acid Catalyzed Asymmetric Cyanohydrin Synthesis. Chemical Reviews, 2008-12-10, roč. 108, čís. 12, s. 5146–5226. Dostupné online [cit. 2022-09-19]. ISSN 0009-2665. DOI: 10.1021/cr800255k. (po anglicky)
- ↑ LIDY, Werner; SUNDERMEYER, Wolfgang. Spaltungsreaktionen des Trimethylsilylcyanids, eine neue Darstellungsmethode für O ‐(Trimethylsilyl)cyanhydrine. Chemische Berichte, 1973-02, roč. 106, čís. 2, s. 587–593. Dostupné online [cit. 2022-09-19]. ISSN 0009-2940. DOI: 10.1002/cber.19731060224. (po anglicky)
- ↑ SCHOLL, Matthias; LIM, Chee-Kiang; FU, Gregory C.. Convenient and efficient conversion of aldehydes to acylated cyanohydrins using tributyltin cyanide as catalyst. The Journal of Organic Chemistry, 1995-09, roč. 60, čís. 19, s. 6229–6231. Dostupné online [cit. 2022-09-19]. ISSN 0022-3263. DOI: 10.1021/jo00124a052. (po anglicky)
- ↑ YONEDA, Ryuji; HARUSAWA, Shinya; KURIHARA, Takushi. Cyano phosphate: an efficient intermediate for the chemoselective conversion of carbonyl compounds to nitriles. The Journal of Organic Chemistry, 1991-03, roč. 56, čís. 5, s. 1827–1832. Dostupné online [cit. 2022-09-19]. ISSN 0022-3263. DOI: 10.1021/jo00005a031. (po anglicky)
- ↑ JUHL, Martin; PETERSEN, Allan R.; LEE, Ji‐Woong. CO 2 ‐Enabled Cyanohydrin Synthesis and Facile Iterative Homologation Reactions**. Chemistry – A European Journal, 2021-01-04, roč. 27, čís. 1, s. 228–232. Dostupné online [cit. 2022-09-19]. ISSN 0947-6539. DOI: 10.1002/chem.202003623. (po anglicky)
- ↑ William Bauer, Jr. "Methacrylic Acid and Derivatives" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a16_441. Article Online Posting Date: June 15, 2000
- ↑ Haroutounian, S. A. "Acetone Cyanohydrin" Encyclopedia of Reagents for Organic Synthesis 2001, John Wiley & Sons. DOI:10.1002/047084289X.ra014
- ↑ Organic Syntheses Procedure [online]. www.orgsyn.org, [cit. 2022-09-19]. Dostupné online. (po anglicky)
Zdroj[upraviť | upraviť zdroj]
Tento článok je čiastočný alebo úplný preklad článku Cyanohydrin na anglickej Wikipédii.