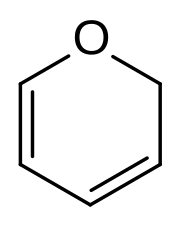
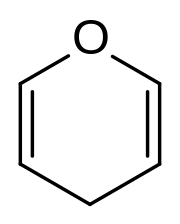
Pyrán
| 2H-Pyrán, 4H-Pyrán | |
 | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C5H6O |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 82,102 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 289-66-7 (2H)
289-65-6 (4H) |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Pyrán alebo oxín je heterocyklická zlúčenina, ktorá má šesťčlenný nearomatický cyklus pozostávajúci z piatich uhlíkov a jedného kyslíka s dvomi dvojitými väzbami. Existujú dva izoméry pyránu, ktoré sa líšia polohou dvojitých väzieb. 2H-pyrán má nasýtený uhlík na pozícii 2, zatiaľ čo 4H-pyrán má nasýtený uhlík na pozícii 4.
4H-Pyrán bol poprvé izolovaný a charakterizovaný v roku 1962 pyrolýzou 2-acetoxy-3,4-dihydro-2H-pyránu.[1] Bol však príliš nestabilný, hlavne na vzduchu. 4H-Pyrán sa jednoducho disproporcionuje na príslušný dihydropyrán a pyryliový ión, ktorý sa ľahko hydrolyzuje vo vodnom médiu.
Aj keď pyrány samotné nie sú v chémii veľmi významné, mnohé ich deriváty sú dôležité biologické molekuly, ako napríklad pyránoflavonoidy.
Názov pyrán sa často používa i pre jeho nasýtený analóg, ktorý sa správne označuje ako tetrahydropyrán (oxán). Monosacharidy, ktoré obsahujú šesťčlenný kruh, sú známe ako pyranózy.
Referencie[upraviť | upraviť zdroj]
- ↑ γ-Pyran. Journal of the American Chemical Society, 1962, s. 2452–2453. DOI: 10.1021/ja00871a037.
Pozri aj[upraviť | upraviť zdroj]
Zdroj[upraviť | upraviť zdroj]
Tento článok je čiastočný alebo úplný preklad článku Pyran na anglickej Wikipédii.
