Skladanie bielkovín
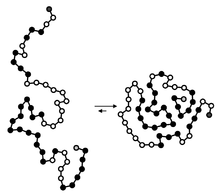
Skladanie bielkovín/proteínov[1][2] (iné názvy: zbaľovanie/zbalenie bielkovín/proteínov[1][3], folding (proteínov/bielkovín)[4][5], zvinovanie/zvinutie bielkovín/proteínov[6][7][8], pozohýnanie bielkovín/proteínov (v priestore)[9][5][4]) je proces, počas ktorého bielkovina nadobúda jej termodynamicky najstabilnejšiu a zároveň funkčnú, tzv. natívnu konformáciu (tvar). Počas zbaľovania jednotlivé časti bielkoviny vytvárajú sekundárne štruktúry, ktoré navzájom interagujú a vytvárajú terciárnu štruktúru, čiže definitívne usporiadanie danej bielkoviny v trojrozmernom priestore.
In vivo začína proces skladania kotranslačne, čiže už počas translácie bielkoviny na ribozóme. Bielkoviny, ktoré sa nestihnú zbaliť kotranslačne, sa môžu zbaliť spontánne, prípadne kotranslokačne, čiže počas prenosu do inej časti bunky, typicky do endoplazmatického retikula. Väčšina bielkovín však nie je schopných zbaliť sa spontánne a pomáhajú im v tom špecializované molekuly, tzv. šaperóny. Tieto molekuly sú tiež schopné pomôcť s foldingom zle zbalených bielkovín, čiže takých, ktoré nadobudli termodynamicky stabilnú, ale nie natívnu konformáciu.
In vitro je možné pozorovať kotranslačné skladanie v tzv. cell-free (bezbunkových) expresných systémoch, čo sú nástroje molekulárnej biológie, ktoré slúžia na expresiu bielkovín z DNA bez použitia buniek. Trochu iným spôsobom, ale s rovnakým výsledkom, prebieha tzv. renaturácia, čo je zbaľovanie bielkoviny, ktorá bola denaturovaná. Denaturácia bielkovín znamená poškodenie ich natívnej konformácie (väčšinou pomocou zvýšenej teploty alebo chemických činidiel) a ich renaturáciu je možné v niektorých prípadoch dosiahnuť odstránením daného denaturačného faktoru. Nie všetky bielkoviny je možné renaturovať a v takom prípade ide o ireverzibilnú (čiže nevratnú) denaturáciu.
Zle zbalené proteíny sú v bunkách odstraňované fyziologickými mechanizmami proteolýzy, predovšetkým na proteazóme a v lyzozóme. Ak nie sú zle zbalené proteíny systematicky odstraňované, môže viesť takýto stav k vážnejším patologickým javom, ktoré sa prejavujú typicky ako neurodegeneratívne ochorenia (napr. Parkinsonova choroba), ale môžu dať počiatok aj vzniku alergií.
Nie všetky bielkoviny sú funkčné ako zbalené. Skupina tzv. vnútorne neusporiadaných proteínov nemá žiadnu definovanú terciárnu štruktúru, napriek tomu zastávajú svoje funkcie. Niektoré vnútorne neusporiadané proteíny získavajú terciárnu štruktúru väzbou ligandu, iné vôbec. Neusporiadanosť im zabezpečuje funkčnú variabilitu a schopnosť viazať viacero rôznych ligandov. Mnohokrát ide o jedny z najdôležitejších proteínov riadiacich bunkový cyklus, napr. proteíny p27 a p55.[10]
Anfinsenova dogma[upraviť | upraviť zdroj]
Anfinsenova dogma je súbor troch hlavných postulátov, ktoré určil americký biochemik Christian B. Anfinsen v 50. rokoch 20. storočia na základe jeho štúdia renaturácie enzýmu ribonukleázy A. Anfinsen pozoroval deaktiváciu tohto enzýmu v roztoku močoviny s redukčným činidlom. Po tom, čo močovinu a redukčné činidlo odstránil, bola aktivita enzýmu obnovená. Tento pokus bol neskôr zopakovaný aj s chemicky syntetizovanou ribonukleázou A, čím sa odstránili pochybnosti, že by mohol byť Anfinsenov experiment ovplyvnený nečistotami v roztoku po izolácii enzýmu.[10][11]
Anfinsenov experiment bol prvým dôkazom, že sekvencia polypeptidového reťazca aminokyselín je dostatočnou informáciou na to, aby reťazec nadobudol konkrétnu trojrozmernú konfiguráciu – čiže terciárnu štruktúru. Anfinsen na základe výsledkov experimentu zhrnul tri základné body:
- Jedinečnosť – Daná sekvencia aminokyselín môže nadobudnúť iba jednu konfiguráciu s najnižšou Gibbsovou energiou, nemôžu existovať dve a viac usporiadaním odlišných, ale energeticky najvýhodnejších konfigurácií tej istej sekvencie aminokyselín v polypeptidovom reťazci.
- Stabilita – Malé zmeny v prostredí (ako zmena pH, teploty a koncentrácie chemických látok) nemôžu spôsobiť zmenu konfigurácie trojrozmernej štruktúry bielkoviny.
- Kinetická dostupnosť – Proces skladania bielkoviny musí prebiehať "hladko", inak povedané, počas skladania nesmú vznikať vysoko usporiadané a komplexné útvary.
Neskôr sa ukázalo, že Anfinsenova dogma platí len pre menšinu proteínov. V skutočnosti je schopných renaturácie len málo proteínov, takisto je aj počet bielkovín schopných zbaliť sa spontánne in vivo v menšine. Mnohé bielkoviny potrebujú na skladanie pomocné molekuly (šaperóny) a ďalšie enzýmy. Ďalšou výnimkou sú prióny, ktoré môžu nadobudnúť termodynamicky stabilnú konformáciu, ktorá ale nie je natívna.[11]
Levinthalov paradox[upraviť | upraviť zdroj]
Levinthalov paradox je myšlienkový experiment, ktorý taktiež odporuje Anfinsenovej dogme. Vyslovil ho v roku 1969 americký molekulárny biológ Cyrus Levinthal. Jeho myšlienkový experiment je založený na obrovskom počte rôznych konformácií, ktoré potrebuje bielkovina "odskúšať", až kým dosiahne tú termodynamicky najstabilnejšiu. Napríklad, polypeptidový reťazec tvorený 100 aminokyselinami má 99 peptidových väzieb a teda 198 uhlov φ a Ψ. Ak môže každý z týchto uhlov nadobudnúť jednu z troch stabilných konformácií, môže proteín nadobudnúť 3198 (čiže 2,95x1094) rôznych celkových konformácií. Ak by "vyskúšanie" jednej konformácie trvalo 10−13 sekundy (čo je čas jednej molekulovej vibrácie), čas potrebný na zbalenie takéhoto polypeptidového reťazca by bol 2,95x1081 sekúnd, čo je 9,36x1073 rokov a to je výrazne dlhšie, ako vek vesmíru. Z toho vyplýva, že skladanie bielkovín nemôže byť čisto náhodný proces.[10][12]
V skutočnosti trvá zloženie 100 aminokyselín dlhého polypeptidového reťazca približne 5 sekúnd a Levinthalov paradox bol v priebehu ďalších rokov čiastočne vysvetlený. Z tohto hľadiska bol dôležitý objav, že skladanie prebieha kotranslačne. To znamená, že N-koncová časť reťazca bielkoviny, ktorá ešte nie je dosyntetizovaná, nie je ovplyvnená týmito ešte nenasyntetizovanými úsekmi a zbaľuje sa od nich nezávisle. Dôležitým objavom bol aj veľký vplyv hydrofóbneho efektu, pre ktorý sa vo vnútornej časti molekuly bielkoviny vytvára tzv. hydrofóbne jadro, ktoré má veľký vplyv na jej stabilitu. Ďalším vysvetlením Levinthalovho paradoxu je hierarchická časová následnosť zbaľovania – rýchlejšie procesy zbaľovania ovplyvňujú procesy pomalšie. Najrýchlejšie sa skladajú sekundárne štruktúry (alfa-hélix a beta-skladaný list), blízke sekundárne štruktúry následne tvoria stabilné tzv. foldy. Následne medzi sebou interagujú jednotlivé foldy a postupne sa stabilizuje celá terciárna štruktúra.[10][13]
Termodynamika skladania[upraviť | upraviť zdroj]
Ako každý chemický proces, aj proces skladania bielkovín popisuje termodynamika pomocou veličiny zvanej Gibbsova energia (G). Gibbsova energia je veličina, ktorá hovorí o stabilite danej molekuly alebo komplexu molekúl. Ak je Gibbsova energia produktov chemického deja nižšia ako Gibbsova energia reaktantov (rozdiel Gibbsových energií ΔG je teda záporný), sú produkty termodynamicky stabilnejšie. Gibbsova energia je pri konštantnom tlaku a teplote definovaná ako
- ,
kde
- G je Gibbsova energia (jednotka SI: Joule)
- H je entalpia (jednotka SI: Joule)
- T je teplota (jednotka SI: Kelvin)
- S je entropia (jednotka SI: Joule na Kelvin).
Entropia je veličina, ktorá charakterizuje neusporiadanosť v systéme – čím je neusporiadanosť väčšia, tým je entropia väčšia a tým je systém termodynamicky stabilnejší. Entalpia charakterizuje príspevok väzieb – čím je chemická väzba (jej väzbová energia) silnejšia (väčšia), tým je entalpia nižšia a systém termodynamicky stabilnejší. Pre výpočet celkovej zmeny Gibbsovej energie ΔG je potrebné brať do úvahy aj vodu, ktorá in vivo a aj in vitro vytvára okolné prostredie bielkoviny a interaguje s ňou:
Každý člen tejto rovnice vplýva na celkovú zmenu Gibbsovej energie bielkoviny počas jej skladania:
- Člen závisí na charaktere postranných reťazcov aminokyselinových zvyškov v polypeptidovom reťazci, väčšinou je však mierne kladný, pretože postranné reťazce interagujú lepšie s vodou (nezbalený stav) ako sami so sebou (zbalený stav).
- Člen je záporný, pretože molekuly vody radšej interagujú sami so sebou (bielkovina zbalená) ako s postrannými zvyškami predovšetkým hydrofóbnych aminokyselín (bielkovina nezbalená).
- Člen je veľký a kladný, pretože entropia (neusporiadanosť) bielkoviny je omnoho vyššia pre nezbalený stav ako pre stav zbalený.
- Člen je veľký a záporný, pretože keď je bielkovina nezbalená, tak má hydrofóbne aminokyselinové zvyšky v kontakte s molekulami vody. Molekuly vody sa okolo týchto aminokyselinových zvyškov orientujú určitým spôsobom a vytvárajú výrazne organizovanú štruktúru s vysokou usporiadanosťou a teda nízkou entropiou.
skladanie proteínov je teda z termodynamického hľadiska najviac ovplyvnené entropickým efektom, pretože molekuly vody sú okolo zbaleného proteínu omnoho menej usporiadané ako okolo proteínu nezbaleného. Tento efekt je častejšie nazývaný ako hydrofóbny efekt alebo hydrofóbna interakcia, pretože v konečnom dôsledku spôsobuje agregáciu nepolárnych postranných reťazcov vo vnútri bielkoviny a vystavenie polárnych postranných reťazcov na jej povrch. K zbaľovaniu tiež prispievajú disulfidické mostíky, soľné mostíky a van der Waalsove interacie.[10][14]
Lievik skladania[upraviť | upraviť zdroj]

Lievik skladania (anglicky folding funnel) je náčrt procesu skladania proteínov z hľadiska termodynamiky. Nezbalených stavov je mnoho a sú charakteristické relatívne veľkou Gibbsovou energiou. Počas skladania sa Gibbsova energia znižuje a s ňou aj počet možných konformačných stavov, ktoré je možné nadobudnúť. Na spodku lievika je termodynamicky najstabilnejší stav, ktorý korešponduje s natívnym stavom bielkoviny. Hĺbka lievika naznačuje, do akej miery je natívny stav bielkoviny stabilný oproti denaturovaným stavom a jeho šírka naznačuje konformačnú entropiu stavov o danej energii.
Jednotlivé lieviky majú pre každý proteín iný tvar. Ten záleží na množstve možných konfigurácií, ktoré sú závislé na tom, aká je zložitá cesta skladania bielkoviny, či existujú semistabilné intermediáty skladania a či majú tieto intermediáty potenciálnu schopnosť tvoriť zhluky (agregovať). Napríklad pre bielkoviny, ktoré na poskladanie potrebujú pomoc od šaperónov (pozri nižšie) je typický výskyt viacerých hlbších lokálnych energetických miním, v ktorých sa môže daná bielkovina počas skladania "zaseknúť". Naopak, pre bielkoviny, ktoré je možné renaturovať, je typický hladký povrch lievika.[10]
Šaperóny[upraviť | upraviť zdroj]
Väčšina bielkovín nie je schopných zbaliť sa spontánne a potrebujú pomoc od iných bielkovín, ktoré s nimi interagujú a pomáhajú im nadobudnúť natívnu konformáciu. Tieto bielkoviny sa nazývajú šaperóny a väzbou na zbaľované proteíny im vytvárajú mikroprostredie, ktoré im skladanie z termodynamického hľadiska uľahčuje. Známe sú dve hlavné rodiny šaperónov – rodina Hsp70 a šaperoníny.[10][15].
Hsp70[upraviť | upraviť zdroj]
Proteíny z rodiny Hsp70 majú relatívnu molekulovú hmotnosť okolo 70 000 a ich množstvo v bunkách sa zväčšuje po tepelnom šoku, z čoho vychádza ich názov (z angl. Heat shock protein). Tieto bielkoviny sa viažu na hydrofóbne časti bielkovín a tým ich chránia pred denaturáciou teplom a pred vytváraním agregátov s ďalšími syntetizovanými bielkovinami, ktoré ešte nie sú zbalené. Niektoré z nich na druhej strane blokujú skladanie bielkovín, ktoré musia zostať v nezbalenej forme, kým sa dostanú na membránu. Ďalšie sprostredkujú správne poskladanie kvartérnej štruktúry viacreťazcových proteínov. Na nezbalené bielkoviny sa môžu viazať aj viackrát, pričom vždy spotrebujú jednu molekulu ATP. Pre svoju funkciu potrebujú ďalšie menšie molekuly (ako napr. Hsp40). V krajnom prípade aspoň prenášajú polypeptid do šaperonínov.[10]
Šaperoníny[upraviť | upraviť zdroj]

Šaperoníny sú veľké proteínové komplexy, ktoré vo svojom vnútornom priestore uzatvárajú nezbalené polypeptidy a za spotreby ATP sprostredkujú ich zbalenie do natívneho stavu. Bakteriálne šaperoníny sú komplexom proteínov GroEL a GroES, ich analógy v eukaryotických organizmoch sa nazývajú Hsp60. GroEL má tvar sudu, do ktorého je navedený nezbalený polypeptid a v tomto "sude" je z oboch strán uzavretý proteínmi GroES. GroEL následne za pomalej hydrolýzy ATP postupne mení svoju konformáciu a tak núti bielkovinu v jeho vnútri skladať sa. Tento proces trvá približne 10 sekúnd, až kým nie je uvoľnená Jedna z podjednotiek GroES. Ak bielkovina nebola zbalená správne, proces sa môže opakovať.[10]
Enzýmy pri skladaní[upraviť | upraviť zdroj]
Pre skladanie niektorých proteínov sú potrebné enzýmy, ktoré katalyzujú izomeračné reakcie. Takým enzýmom je proteín disulfid izomeráza, ktorá katalyzuje vzájomnú premenu alebo premiešanie disulfidických mostíkov, čiže zánik vytvorený disulfidických mostíkov a vznik nových, medzi inými atómami síry. Tento enzým tak eliminuje medziprodukty skladania so zle spárovanými disulfidickými väzbami. Enzým peptid propyl cis-trans izomeráza katalyzuje izomeráciu medzi cis a trans izomérmi prolínových zvyškov. Prolín v cis konformácii má dôležitú funkciu ako aminokyselina, ktorá ohraničuje sekundárne štruktúry, tvorí tzv. ß-ohyby a v mnoho prípadoch je nezameniteľná pre správnu funkciu bielkoviny.[10]
Eliminácia nesprávne zbalených bielkovín[upraviť | upraviť zdroj]
Napriek vyššie popísaným procesom, ktoré vedú k správnemu skladaniu bielkovín, sú v bunke syntetizované aj bielkoviny zbalené nesprávne. V skutočnosti je viac ako štvrtina všetkých syntetizovaných polypeptidov odstránená pre ich nesprávny folding. V eukaryotických bunkách sú bielkoviny, ktoré sú sekretované do extracelulárneho (mimobunkového) priestoru, zbaľované až v endoplazmatickom retikulu. V stresových podmienkach sa biosyntéza bielkovín v bunke zvyšuje a prevyšuje tak kapacitu endoplazmatického retikula. Bunka na to fyziologicky reaguje zvýšením koncentrácie šaperónov a znížením produkcie proteínov. Proteíny, ktoré sa stihli zbaliť nesprávne ešte pred bunkovou reakciou na ne, môžu byť degradované autofágiou, čo je proces, počas ktorého je vnútorná časť bunky obalená membránou a takto vzniknutá kapsula následne fúzuje (splynie) s lyzozómom, v ktorom sa nachádzajú degradačné enzýmy. Alternatívne môžu byť zle zbalené proteíny ubiquitinylované a zacielené do proteazómu.[10][15]
Amyloidózy[upraviť | upraviť zdroj]
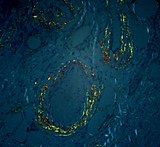
Ak nie sú zle zbalené proteíny odbúravané, môžu agregovať a vytvárať tzv. amyloidné vlákna, ktoré sú tvorené zle zbalenými sekretovanými proteínmi v extracelulárnom priestore. Jedno vlákno má priemer 7 – 10 nm. Pozostávajú z tzv. jadra, ktoré je tvorené agregovanými ß-skladanými listami jednotlivých zle zbalených bielkovín, pričom tieto ß-listy sú kolmé na pozdĺžny smer vlákna a postranných častí bielkovín. Amyloidné vlákna môže vytvoriť mnoho bielkovín a väčšina z nich má štruktúru vlákna stabilizovanú zvýšeným množstvom aromatických aminokyselín. Súbor ochorení, ktoré tieto vlákna spôsobujú, sa nazýva amyloidózy a tie často vznikajú práve mutáciou, pri ktorej sa zamení nejaká aminokyselina z bielkoviny za aromatickú aminokyselinu. Medzi najznámejšie amyloidózy patria tie, ktoré spôsobujú neurodegeneratívne ochorenia, akými sú Alzheimerova choroba, Huntingtonova choroba alebo Parkinsonova choroba.[10]
Priónové ochorenia[upraviť | upraviť zdroj]
Priónové ochorenia, tiež známe pod názvom spongiformné encefalitídy, sú, podobne ako amyloidózy, ochorenia, ktoré vznikajú zlým zbalením proteínu, v tomto prípade tzv. priónového proteínu. Patrí medzi ne Creutzfeldt-Jakobova choroba, Choroba šialených kráv, kuru a iné. Zle zbalený priónový proteín tvorý štruktúry podobné amyloidným vláknam. Navyše, zle zbalená forma tohto proteínu spôsobuje zmenu správne zbalených priónových proteínov na ďalšie zle zbalené proteíny. Fyziologická funkcia priónového proteínu však nie je známa.[10].
Referencie[upraviť | upraviť zdroj]
- ↑ a b DOBROTA, Dušan, a kol. Lekárska biochémia : vysokoškolská učebnica. 1. slov. vyd. Martin : Osveta, 2012. 723 s. ISBN 978-80-8063-293-9. S. 448.
- ↑ SYLABY Z BIOCHÉMIE (ZUBNÉ LEK.) [online]. Košice: Univerzita Pavla Jozefa Šafárika v Košiciach, [cit. 2015-04-04]. Dostupné online.
- ↑ Proteíny [online]. Košice: Univerzita Pavla Jozefa Šafárika v Košiciach, [cit. 2015-04-04]. Dostupné online.
- ↑ a b proteín. In: Encyklopédia medicíny, 13. zväzok. Bratislava : Asklepios, 2003. ISBN 80-7167-021-9.
- ↑ a b folding proteínov [online]. Bratislava: Slovenská lekárska knižnica, [cit. 2015-04-04]. Dostupné online.
- ↑ PARNICA, Jozef. FYZIKA BIELKOVÍN [online]. [Cit. 2015-04-04]. Dostupné online. Archivované 2015-04-09 z originálu.
- ↑ KOVÁČ, Ladislav. Bioenergetika: kľúč k pochopeniu mozgu a mysle. In: Modely mysle. 1. vyd. Bratislava : Európa, 2008. ISBN 978-80-89111-34-3. s. 100-126. dostupné online
- ↑ svinování bílkovin{2} [online]. Praha: VŠCHT, [cit. 2015-04-04]. V knižnej podobe Biochemické pojmy - výkladový slovník, ISBN 80-7080-551-X. Dostupné online. (po česky)
- ↑ KALIŇÁK, Michal. Tvorba protilátok [online]. Bratislava: Fakulta chemickej a potravinárskej technológie, 4.4.2015, [cit. 2015-04-04]. Dostupné online. Archivované 2015-04-09 z originálu.
- ↑ a b c d e f g h i j k l m NELSON, David L.; COX, Michael M.. Lehninger Principles of Biochemistry. 6. vyd. New York : W. H. Freeman and Company, 2013. ISBN 978-1-4641-0962-1. (anglicky)
- ↑ a b Anfinsen CB. Principles that govern the folding of protein chains. Science, 1973, s. 223 – 230. DOI: 10.1126/science.181.4096.223. PMID 4124164.
- ↑ LEVINTHAL, Cyrus. Are there pathways for protein folding?. Journal de Chimie Physique et de Physico-Chimie Biologique, 1968, s. 44 – 45. Dostupné online. Archivované 2009-09-02 na Wayback Machine
- ↑ FEDOROV, Alexej N.; BALDWIN, Thomas O.. Cotranslational Protein Folding. The Journal of Biological Chemistry, 1997, s. 32715–32718.
- ↑ KODÍČEK, Milan; KARPENKO, Vladimír. Biofysikální chemie. 2. vyd. Praha : ACADEMIA, 2013. ISBN 978-80-200-2241-7. (česky)
- ↑ a b VOET, Donald; VOET, Judith G.. Biochemistry. 4. vyd. Hoboken, NJ : Wiley, 2010. ISBN 978-0470917459. (anglicky)
- ↑ Flaherty KM, DeLuca-Flaherty C, McKay DB. Three-dimensional structure of the ATPase fragment of a 70K heat-shock cognate protein. Nature, August 1990, s. 623 – 8. DOI: 10.1038/346623a0. PMID 2143562.






