Uhličitan vápenatý
| Uhličitan vápenatý | |||||||
 | |||||||
 | |||||||
| Všeobecné vlastnosti | |||||||
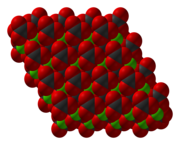
| Sumárny vzorec | CaCO3 | ||||||
| Vzhľad | biela tuhá látka | ||||||
| Fyzikálne vlastnosti | |||||||
| Molekulová hmotnosť | 100,0869 g/mol | ||||||
| Teplota topenia | 1 339 °C | ||||||
| Teplota varu | rozklad | ||||||
| Hustota | 2,711 g/cm3 | ||||||
| |||||||
| Ďalšie informácie | |||||||
| Číslo CAS | 471-34-1 | ||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||
Uhličitan vápenatý (CaCO3) je chemická zlúčenina, ktorá sa v prírode vyskytuje ako minerály kalcit a aragonit, alebo ako hlavná súčasť vápenca – usadenej horniny prevažne biologického pôvodu.
Vlastnosti[upraviť | upraviť zdroj]
Je vo vode nerozpustný, ale reakciou s vodou nasýtenou rozpusteným oxidom uhličitým vniká rozpustný hydrogénuhličitan vápenatý.
- CaCO3 + CO2 + H2O → Ca(HCO3)2
Zahrievaním na 825 °C bez prístupu vzduchu sa mení na nehasené vápno (oxid vápenatý, CaO):
- CaCO3 → CaO + CO2
Je stály v alkalickom prostredí, s kyselinami sa rozkladá za vzniku oxidu uhličitého.
- CaCO3 + 2 H+ → Ca2+ + H2O + CO2
Krieda[upraviť | upraviť zdroj]
Pod názvom krieda sa používa ako biely pigment v maliarstve. Predávajú sa rôzne druhy:
- plavená krieda – získava sa mletím a plavením kriedových hornín, obsahuje aj vápenaté a horečnaté fosfáty
- mletá krieda – podobá sa na plavenú kriedu, má však väčšiu zrnitosť
- bolonská krieda
- šampanská krieda
- umelá krieda – vyrába sa zrážaním z roztoku chloridu vápenatého, je čistejšia a jemnejšia než prírodná krieda
Pozri aj[upraviť | upraviť zdroj]
Iné projekty[upraviť | upraviť zdroj]
 Commons ponúka multimediálne súbory na tému Uhličitan vápenatý
Commons ponúka multimediálne súbory na tému Uhličitan vápenatý

