Heterocyklická zlúčenina: Rozdiel medzi revíziami
d +portál Chémia |
|||
| Riadok 178: | Riadok 178: | ||
Existuje veľké množstvo zložitejších heterocyklov. Mnohé sú základom [[alkaloidy|alkaloidov]] Tu je prehľad niektorých z nich: |
Existuje veľké množstvo zložitejších heterocyklov. Mnohé sú základom [[alkaloidy|alkaloidov]] Tu je prehľad niektorých z nich: |
||
<gallery> |
<gallery> |
||
Súbor:Pteridin - Pteridine.svg|[[Pteridín]] |
|||
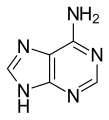
Súbor:Adenine.svg|[[Adenín]] |
|||
Súbor:Guanine chemical structure.png|[[Guanín]] |
|||
image:Pteridin_-_Pteridine.svg|[[Pteridín]] |
|||
Súbor:Thymine chemical structure.png|[[Tymín]] |
|||
image:Adenine.svg|[[Adenín]] |
|||
Súbor:Uracil chemical structure.png|[[Uracil]] |
|||
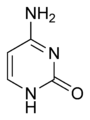
Súbor:Cytosine chemical structure.png|[[Cytozín]] |
|||
image:Thymine_chemical_structure.png|[[Tymín]] |
|||
Súbor:Caffeine.svg|[[Kofeín]] |
|||
image:Uracil_chemical_structure.png|[[Uracil]] |
|||
Súbor:UricAcid.png|[[Kyselina močová]] |
|||
image:Cytosine_chemical_structure.png|[[Cytozín]] |
|||
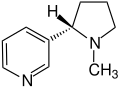
Súbor:Nikotin - Nicotine.svg|[[Nikotín]] |
|||
Súbor:Barbituric acid.png|[[Kyselina barbiturová]] |
|||
image:Nikotin_-_Nicotine.svg|[[Nikotín]] |
|||
image:Barbituric_acid.png|[[Kyselina barbiturová]] |
|||
</gallery> |
</gallery> |
||
Verzia z 22:39, 21. október 2018

Heterocyklická zlúčenina je pomenovanie organickej zlúčeniny, ktorej molekula je tvorená aspoň jedným uhlíkovým cyklom, v ktorom sa však priamo v cykle okrem uhlíka nachádza aj iný prvok, napríklad kyslík, síra, dusík (najčastejšie), vzácnejšie aj fosfor, selén, telúr a iné. Takýto cyklus sa nazýva heterocyklus a neuhlíkový atóm v ňom sa nazýva heteroatóm; slovo heterocyklus sa alternatívne používa aj ako synonymum výrazu heterocyklická zlúčenina.
Delenie heterocyklických zlúčenín
Heterocyklické zlúčeniny možno rozdeliť z viacerých hľadísk, čo vyplýva z toho, že v heterocykle môže byť nielen jeden, ale aj viac heteroatómov, ktoré môžu byť vo vzájomných rôznych polohách. Heterocyklické zlúčeniny môžu obsahovať aj viacej cyklov, z ktorých nie každý (ale aspoň jeden) musí obsahovať heteroatóm.
Zlúčeniny s heteroatómami len jedného prvku, môžeme ich rozdeliť na:
- kyslíkaté
- sírnaté
- dusíkaté
Ak zlúčenina obsahuje len jeden heterocyklus, podľa počtu atómov v tomto cykle rozlišujeme:
- trojčlánkové
- štvorčlánkové
- päťčlánkové
- šesťčlánkové
Ich chemické vlastnosti sú podobné vlastnostiam benzénu.
Využitie
Skoro všetky heterocykly sú prírodného pôvodu. tvoria základné štruktúry živého organizmu. Všetky syntetické heterocykly sa získavajú z ropy.
Trojčlánkové heterocykly

Z trojčlánkových heterocyklov sú stabilné len tie, ktoré obsahujú jeden heteroatóm. V porovnaní s inými heterocyklami sú veľmi reaktívne. Najbežnejšie trojčlánkové heterocykly sú:
| heteroatóm | nasýtený | nenasýtený |
|---|---|---|
| Dusík | aziridín | |
| Kyslík | oxirán (etylénoxid) | |
| Síra | etylénsulfid |
Štvorčlánkové heterocykly

| heteroatóm | nasýtené | nenasýtené |
|---|---|---|
| Dusík | azetidín | |
| Kyslík | oxetán |
Päťčlánkové heterocykly
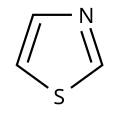
Päťčlánkové s 1 heteroatómom

| heteroatóm | nasýtené | nenasýtené |
|---|---|---|
| Dusík | pyrolidín | pyrol |
| Kyslík | tetrahydrofurán | furán |
| Síra | tetrahydrotiofén | tiofén |
| Arzén | arzol |
Furán

- Hlavný článok, pozri Furán.
V heterocykle obsahuje atóm kyslíka. Je bezfarebný, kvapalný, vo vode málo rozpustný. Zápach má podobný ako chloroform. Obsahuje atóm kyslíka a preto sa ľahko poskytuje voľný elektrón do reakcie. Využíva sa na tvorbu polymérov.
Tiofén

- Hlavný článok, pozri Tiofén.
Nachádza sa v čiernouhoľnom dechte.
Pyrol


Z gréčtiny Phyros - červený. Nachádza sa v dechte, v kostiach, rohovine a prakticky vo všetkých látkach ktoré sú obsiahnuté v bielkovinách. Je veľmi slabá zásada až kyselina. Má schopnosť zafarbiť pravé smrekové drevo na ohnivú červeň aj napriek tomu, že drevo bolo namočené v kyseline chlorovodíkovej (HCl).
Z pyrolového kruhu sa odvodzujú deriváty pyrolu:
- Porfín(aj ako Prolín) (základ pre zlúčeninu HEM (krvné farbivo), tvoriacu hemoglobín)
- 4 hydroxyprolín
- Indol (súčasť indiga, aminokyseliny Tryptofánu a alkaloidov; vôňa ako jazmín)
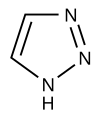
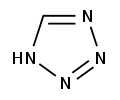
Päťčlánkové s 2 a viac heteroatómami
Šesťčlánkové heterocykly
Šesťčlánkové s 1 heteroatómom
| heteroatóm | nasýtené | nenasýtené |
|---|---|---|
| Dusík | piperidín | pyridín |
| Kyslík | pyrán | |
| Síra | tiopyrán |
Pyridín
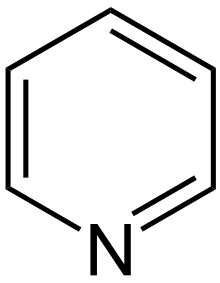
- Hlavný článok, pozri Pyridín.
Pyridín je zásaditý, kvapalný a vo vode rozpustný. Nachádza sa v čiernouhoľnom dechte. Zúčastnuje sa na elektrofilných substitúciach. Pyridínový kruh sa nachádza aj napríklad v kyseline barbiturovej, ktorá je súčasťou barbiturátov.
Deriváty pyridínu sú:
Chinolín

- Hlavný článok, pozri Chinolín.
Nachádza sa v dechte. Je zle rozpustný vo vode.
Derivát chinolínu je chinilín.
Šesťčlánkové s 2 a viac heteroatómami
Zložitejšie heterocykly
Existuje veľké množstvo zložitejších heterocyklov. Mnohé sú základom alkaloidov Tu je prehľad niektorých z nich: