Acylácia
Acylácia alebo niekedy alkanoylácia je proces v organickej chémii, v ktorom dochádza k naviazaniu acylovej skupiny (zvyšku od karboxylovej kyseliny) na inú zlúčeninu.[1] Látka, ktorá poskytuje acylovú skupinu, sa nazýva acylačné činidlo.
Acylhalogenidy sa bežne používajú ako acylačné činidlá, pretože pri pôsobení kovových katalyzátorov tvoria silné elektrofily. Friedel-Craftsova acylácia napríklad využíva acetylchlorid (etanoylchlorid), CH3COCl, ako acylačné činidlo a chlorid hlinitý, AlCl3, ako kovový katalyzátor na naviazanie etanoylovej (acetylovej) skupiny na benzén:
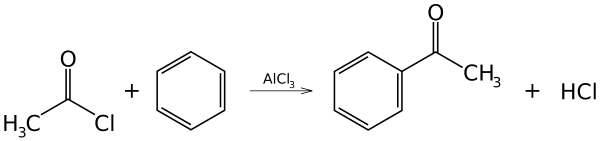
Mechanizmus tejto reakcie je elektrofilná aromatická substitúcia.
Acylhalogenidy a anhydridy karboxylových kyselín sa takisto bežne používajú ako acylačné činidlá. V niektorých prípadoch majú i aktivované estery porovnateľnú reaktivitu. Všetky tieto látky reagujú s amínmi za vzniku amidov a s alkoholmi za vzniku esterov. Tieto reakcie prebiehajú ako nukleofilná acylová substitúcia
Acyláciu je možné využiť na predídenie prešmykom, ktoré bežne prebiehajú pri alkylácii. Pri takomto použití sa využije acylačná reakcia a karbonyl sa potom odstráni pomocou Clemmensenovej redukcie alebo obdobného procesu.[2]
Acylácia v biológii[upraviť | upraviť zdroj]
Acylácia bielkovín je posttranslačná úprava bielkovín, pri ktorej sa na bielkoviny viažu funkčné skupiny cez acylové skupiny. Proteinová acylácia predstavuje mechanizmus, ktorým sa riadi biologická signalizácia.[3] Jeden z dôležitých druhov je acylácia mastnými kyselinami, pri ktore dochádza k naviazaniu mastných kyselín na konkrétne aminokyseliny (procesy ako myristoylácia, palmitoylácia, palmitoleoylácia a iné).[4] Rôzne druhy mastných kyselín sa účastnia acylácie bielkovín.[5] Palmitoleoylácia je druh acylácie, kde dochádza ku kovalentnému naviazaniu jedenkrát nenasýtenej kyseliny palmitoleovej na serín alebo treonín v proteínoch.[6][7] Táto úprava má zjavne dôležitú úlohu v presúvaní a cielení bielkovín a takisto vo funkcii Wnt proteínov.[8][9]
Referencie[upraviť | upraviť zdroj]
- ↑ acylácia. In: BÍNA, Jaroslav. Malá encyklopédia chémie. Bratislava : Obzor, 1981. S. 70.
- ↑ VOLLHARDT, Peter; Neil E. Schore. Organic Chemistry: Structure and Function.. 7th. vyd. New York, NY : W.H. Freeman and Company, 2014. ISBN 978-1-4641-2027-5. S. 714–715.
- ↑ The Biology and Enzymology of Eukaryotic Protein Acylation. Annual Review of Biochemistry, 1988, s. 69–97. DOI: 10.1146/annurev.bi.57.070188.000441. PMID 3052287.
- ↑ Fatty acylation of proteins: New insights into membrane targeting of myristoylated and palmitoylated proteins. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research, 1999, s. 1–16. DOI: 10.1016/S0167-4889(99)00075-0. PMID 10446384.
- ↑ A method for the gross analysis of global protein acylation by gas–liquid chromatography. IUBMB Life, 2019, s. 340–346. ISSN 1521-6551. DOI: 10.1002/iub.1975. PMID 30501005.
- ↑ HANNOUSH, Rami N.. Synthetic protein lipidation. Current Opinion in Chemical Biology, October 2015, s. 39–46. ISSN 1879-0402. DOI: 10.1016/j.cbpa.2015.05.025. PMID 26080277.
- ↑ PELEGRI, Francisco; DANILCHIK, Michael; SUTHERLAND, Ann. Vertebrate development : maternal to zygotic control. Cham, Switzerland : [s.n.], 2016-12-13. ISBN 9783319460956.
- ↑ Wnt lipidation: Roles in trafficking, modulation, and function. Journal of Cellular Physiology, 2018-10-20, s. 8040–8054. ISSN 1097-4652. DOI: 10.1002/jcp.27570. PMID 30341908.
- ↑ Fatty acylation of Wnt proteins. Nature Chemical Biology, February 2016, s. 60–69. ISSN 1552-4469. DOI: 10.1038/nchembio.2005. PMID 26784846.
Pozri aj[upraviť | upraviť zdroj]
Zdroj[upraviť | upraviť zdroj]
Tento článok je čiastočný alebo úplný preklad článku Acylation na anglickej Wikipédii.
