Octan meďnatý: Rozdiel medzi revíziami
d fix. |
gramatika |
||
| Riadok 19: | Riadok 19: | ||
}} |
}} |
||
[[Súbor:Fotografia0230.jpg|thumb|Octan meďnatý]] |
[[Súbor:Fotografia0230.jpg|thumb|Octan meďnatý]] |
||
'''Octan meďnatý''' |
'''Octan meďnatý''' je meďnatá soľ kyseliny octovej - octan. Jedná sa o relatívne rozpustnú tmavo modrú látku, ktorá sa využíva na výrobu organických zlúčenín medi. Je obsiahnutá aj v niektorých nerastoch, a dokonca je aj hlavnou látkou hoganitu.<br /> |
||
==Výroba== |
==Výroba== |
||
Verzia z 16:56, 2. február 2013
| Octan meďnatý | |||||||
[[Obrázok:
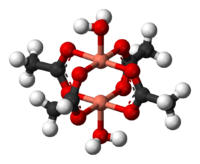 |center|180px|Octan meďnatý]] |center|180px|Octan meďnatý]] | |||||||
| Všeobecné vlastnosti | |||||||
| Systematický názov | ethanoát meďnatý | ||||||
| Fyzikálne vlastnosti | |||||||
| Teplota topenia | 115 °C, 388 K, 239 °F | ||||||
| Teplota varu | 240 °C, 513 K, 464 °F | ||||||
| Hustota | 1,88 g/cm³ (pevný) | ||||||
| Rozpustnosť | 6,8 g/100 ml (25 °C)
20 g/100 ml v horúcej vode, rozpustný v etanole, mierne rozpustný v glycerole a éteri. | ||||||
| |||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||

Octan meďnatý je meďnatá soľ kyseliny octovej - octan. Jedná sa o relatívne rozpustnú tmavo modrú látku, ktorá sa využíva na výrobu organických zlúčenín medi. Je obsiahnutá aj v niektorých nerastoch, a dokonca je aj hlavnou látkou hoganitu.
Výroba
Meď, na rozdiel od niektorých iných kovov, ako je napríklad železo, nereaguje s kyselinami, pretože meď je podľa Beketovovej rady kovov ušľachtilý kov. Preto je výroba pomerne obtiažna.
Priemyselne sa vyrába elektrolýzou octanu vápenatého medenými elektródami, roztok sa nesmie miešať, a nakoniec sa odsaje roztok octanu meďnatého.
Laboratórne možné vyrábať z kyseliny octovej a medi a peroxidu vodíka.
2 CH3COOH + H2O2 + Cu → 2 H2O + Cu (CH3COO) 2
Prípadne je možné vyrábať z oxidu meďnatého alebo uhličitanu meďnatého a kyseliny octovej
2 CH3COOH + CuO → 2 H2O + Cu (CH3COO) 2
2 CH3COOH + CuCO3 → 2 H2O + Cu (CH3COO) 2 + CO2
Reakcie
Octan meďnatý reaguje s peroxidom vodíka, dochádza k rozpadu na nerozpustný oxid meďnatý, preto sa musia pri výrobe za pomocou peroxidu veľmi presne merať a počítať, ale pri prípadnej chybe možno oxid meďnatý zase nechať zreagovať, viď vyššie.
Octan meďnatý reaguje s uhličitanom sodným a kyselinou acetylsalicilovou (aspirínom) za vzniku acetylsalicilátu meďnatého, čo je nerozpustné modré farbivo.
Z octanu meďnatého možno vyrábať aj napríklad dusičnan meďnatý, pričom vzniká však aj octan draselný, a tieto 2 látky sa od seba pomerne ťažko oddeľujú. Reakcia prebieha podľa rovnice:
Cu (CH3COO) 2 + 2 KNO3 → Cu (NO3) 2 + 2 KCH3COO
Octan meďnatý sa používa na výrobu organických zlúčenín medi, a tiež ako katalyzátor, napríklad umožňuje horenie cukru.
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Octan měďnatý na českej Wikipédii.

