Glycerol
| Glycerol | |||||||
 | |||||||
 | |||||||
| Všeobecné vlastnosti | |||||||
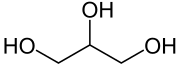
| Sumárny vzorec | C3H8O3 | ||||||
| Synonymá | propan-1,2,3-triol | ||||||
| Fyzikálne vlastnosti | |||||||
| Molárna hmotnosť | 92,0932 g/mol | ||||||
| Teplota topenia | 17,8 °C | ||||||
| Teplota varu | 290 °C | ||||||
| Hustota | 1,26 g/cm³ | ||||||
| |||||||
| Ďalšie informácie | |||||||
| Číslo CAS | 56-81-5 | ||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||
Glycerol, alebo glycerín, systematickým názvom propán-1,2,3-triol, je hygroskopická bezfarebná viskózna kvapalina bez zápachu, sladkej chuti. Je dôležitou biogénnou organickou zlúčeninou, lebo je vo forme svojich esterov súčasťou tukov.
Chemické a fyzikálne vlastnosti[upraviť | upraviť zdroj]
Glycerol je trojsýtny alkohol. Jeho oxidáciou vzniká celý rad látok. Šetrnou oxidáciou jednej primárnej alkoholickej skupiny vzniká jednoduchý monosacharid, aldotrióza glyceraldehyd
- 2 HO-CH2-CH(OH)-CH2-OH + 2 O2 → 2 HO-CH2-CH(OH)-CHO + H2O.
Naopak oxidáciou sekundárnej alkoholickej skupiny vzniká iný monosacharid, ketotrióza dihydroxyaceton
- 2 HO-CH2-CH(OH)-CH2-OH + 2 O2 → 2 HO-CH2-CO- CH2-OH + H2O.
Plnou oxidáciou jednej primárnej alkoholickej skupiny dostaneme kyselinu glycerovú
- HO-CH2-CH(OH)-CH2-OH + O2 → HO-CH2-CH(OH)-COOH + H2O.
Úplnou oxidáciou oboch primárnych alkoholických skupín vzniká kyselina tartronová
- HO-CH2-CH(OH)-CH2-OH + 2 O2 → HOOC-CH(OH)-COOH + 2 H2O.
Úplnou oxidáciou vzniká najjednoduchšia ketodikyselina, kyselina mesoxalová
- 2 HO-CH2-CH(OH)-CH2-OH + 5 O2 → 2 HOOC-CO-COOH + 6 H2O.
Zahrievaný bez prístupu vzduchu odštepuje vodu a mení sa na nenasýtený aldehyd akrolein (propenal)
- HO-CH2-CH(OH)-CH2-OH → H2C=CH-CH=O + 2 H2O.
Pôsobením nitračných činidiel (napr. zmesi koncentrovanej kyseliny dusičnej a kyseliny sírovej) na glycerol vzniká trinitrát glycerolu, známejší pod názvom nitroglycerín
- HO-CH2-CH(OH)-CH2-OH + HNO3 → O2NO-CH2-CH(ONO2)- CH2-ONO2 + 3 H2O,
ktorý je zložkou radu výbušnín (napr. dynamitu) a strelivín (napr. bezdymného strelného prachu).
Vďaka prítomnosti hydroxylových skupín je molekula glycerolu polárna a preto sa neobmedzene miesi s vodou a jednoduchými alkoholmi (napr. metanolom a etanolom). V nepolárnych rozpúšťadlách (napr. benzín) sa nerozpúšťa.
Výroba[upraviť | upraviť zdroj]
Glycerol vzniká pri saponifikácii alebo transesterifikácii.
Saponifikácia[upraviť | upraviť zdroj]
Hlavným zdrojom glycerolu boli prírodné tuky. Pri výrobe mydla sa pôsobením hydroxidu sodného alebo draselného tuky štepia na glycerol a zmes alkalických solí alifatických kyselín, ktoré sú podstatou mydiel:
Transesterifikácia[upraviť | upraviť zdroj]
Pri výrobe bionafty je glycerol vedľajším produktom v podiele asi 10 %. So vzrastajúcim objemom výroby bionafty vo svete tak vzrastá aj objem vyrobeného glycerolu.
Biochémia[upraviť | upraviť zdroj]

Glycerol vzniká vedľa etanolu v procese kvasenia glukózy z 1,3-dihydroxyacetonu, resp. 1,3-dihydroxyacetonfosfátu, ktorý je bežným produktom štiepenia glukózy enzýmatickou redukciou redukovanou formou β-nikotinamidadenindinukleotidu (NADH) za prítomnosti glycerolhydrogenasy.
Preto je tiež vedľajším produktom prípravy etanolu z glukózy fermentáciou kvasinkami Saccharomyces cerevisiae. Keď prebieha kvasenie glukózy za prítomnosti väčšieho množstva siričitanov, blokuje sa čiastočne redukcia acetaldehydu na etanol a vo výslednej zmesi sa zvýši obsah glycerolu. Podobne možno produkciu glycerolu na úkor etanolu zvýšiť, keď prebieha fermentácia v neutrálnom alebo slabo zásaditom prostredí.
Omnoho väčšiu produkcie glycerolu možno však dosiahnuť pri použití iných druhov mikroorganizmov, napr. Debaryomyces mogii, Saccharomyces rouxii, Saccharomyces mellis, Pichia miso, Pichia farinosa, Torulopsis magnoliae, Zygosaccharomyces acidificiens a i.
Fyziologické pôsobenie[upraviť | upraviť zdroj]
Glycerol je slabo jedovatý. V menších dávkach spôsobuje bolesti hlavy, žalúdočné problémy a zvracanie. Vo väčších dávkach môže spôsobiť poškodenie pečene. Najnižšia toxická dávka podaná orálne u človeka činí približne LDLo = 1,5 g/kg živej hmotnosti, čo znamená, že priemerný človek by ho musel požiť najmenej 90 až 120 g, aby sa u neho prejavili symptómy otravy. V nízkych koncentráciách je prakticky neškodný.
V zriedenom stave sa používa k zvlhčovaniu pokožky a slizníc, lebo viaže atmosférickú vlhkosť a tým ju prenáša do povrchu tela; naopak použitie čistého glycerínu je nevhodné, pretože naopak z pokožky odčerpáva vlhkosť a tým ju vysušuje.
Použitie[upraviť | upraviť zdroj]
Glycerol sa používa o. i. v kozmetických výrobkoch, hlavne ako prísada v hydratačných krémoch a mydlách, ako prísada do zubných pást, pri výrobe plastických hmôt hlavne ako zmäkčovadlo, liečiv, žuvačiek, pást, farbív a výbušnín. Používa sa tiež pri výrobe bezvodého etanolu pre odstránenie prímesi vody.
Je súčasťou nemrznúcich zmesí, väčšinou v kombinácii s etylénglykolom.
V potravinárskom priemysle sa užíva ako prísada pre úpravu nápojov a menej kvalitných vín, ako sladidlo napr. v šľahačkách v bombičkách, ako zmäkčovadlo želé a iných cukroviniek a pod.
Ako súčasť potravín má označenie E 422.
V lekárstve sa užíva pri liečbe opuchov mozgu ako prísada infúzií, na znižovanie vnútroočného tlaku, pri zápchach, na zmäkčenie stolice vo forme glycerínových čapíkov alebo ako súčasť klystíru.
Pôvod mena[upraviť | upraviť zdroj]
Názov je odvodený od dvoch význačných vlastností glycerolu, a to jeho sladkej chuti a značnej viskozity. Základom sú grécke slovo γλυκύς, glykys, po slovensky sladký a latinské slovo cera, tj. vosk.

