Enzým: Rozdiel medzi revíziami
d robot Pridal: sw:Kimeng'enya |
|||
| Riadok 71: | Riadok 71: | ||
== Externé odkazy == |
== Externé odkazy == |
||
* [http://www.chem.qmul.ac.uk/iubmb/enzyme/ Názvoslovie enzýmov] (en) |
* [http://www.chem.qmul.ac.uk/iubmb/enzyme/ Názvoslovie enzýmov] (en) |
||
* [http://www.brenda-enzymes.org BRENDA] (en) |
|||
Verzia z 09:28, 13. január 2009
Enzým (z gr. εν- en- „v” a ζύμη zýme „kvas”) je proteín, ktorý katalyzuje chemickú reakciu.
Enzýmy zohrávajú kľúčovú rolu v metabolizme všetkých živých organizmov. Takmer všetky biochemické reakcie, od trávenia (napr. pepsín) až po kopírovanie genetickej informácie (DNA polymeráza), sú katalyzované enzýmami.
Náuka o enzýmoch sa nazýva enzymológia.
Názvoslovie
Názvoslovie enzýmov sa prispôsobuje návrhu Medzinárodnej únie pre biochémiu a molekulárnu biológiu, ktorá v roku 1955 vytvorila Medzinárodnú komisiu pre enzýmy (International Commission on Enzymes alebo skrátene Enzyme Commission, EC) s cieľom systematicky klasifikovať a pomenovať enzýmy a koenzýmy, ich jednotku aktivity a štandardné stanovovacie postupy a symboly na popis enzýmovej kinetiky.
Na návrh komisie vznikli dva typy názvoslovia - systémové a triviálne - ktoré sa zakladajú na type reakcie, ktorú enzým katalyzuje. Systémový názov dostávajú tie enzýmy, u ktorých je dostatočne známy mechanizmus reakcie. Každý enzým má pridelený presný názov a tzv. EC-kód na základe desatinného triedenia. V názve enzýmu je uvedený substrát, výraz charakterizujúci typ reakcie a prípona -áza. Vo vydaní z roku 1992 obsahuje zoznam 3 196 enzýmov.
Desatinné triedenie
| Klasifikácia enzýmov | ||
|---|---|---|
| Základná trieda | Názov | Katalyzovaná reakcia |
| EC 1 | oxidoreduktázy | oxidačno-redukčné reakcie |
| EC 2 | transferázy | prenos skupín atómov medzi molekulami |
| EC 3 | hydrolázy | hydrolytické štiepenie chemickej väzby |
| EC 4 | lyázy | nehydrolytické štiepenie chemickej väzby |
| EC 5 | izomerázy | zmeny substrátu v rámci molekuly |
| EC 6 | ligázy | vznik chemickej väzby za súčasného štiepenia makroergickej väzby |
Mechanizmus enzýmovej reakcie
Má sa za to, že enzýmová reakcia prebieha v niekoľkých reverzibilných stupňoch
- Vznik komplexu enzým–substrát
- E + S ↔ ES
- Aktivácia komplexu enzým–substrát
- ES ↔ ES*
- Premena substrátu na produkt
- ES* ↔ EP
- Disociácia enzýmu a produktu
- EP ↔ E + P
Po zjednodušení dostaneme kinetickú rovnicu, v ktorej vystupujú rýchlostné konštantny jednotlivých reakcií ():
Na začiatku reakcie predpokladáme, že koncentrácia produktu je veľmi nízka a rýchlosť reakcie bude determinovaná koncentráciou komplexu enzým–substrát a maximálna bude vtedy, ak sa všetok enzým bude viazať vo forme komplexu ES.
Michaelis–Mentenovej rovnica
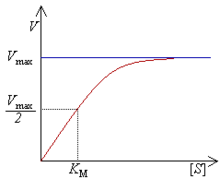
Merania rýchlosti enzýmovej reakcie ukázali, že zvyšovanie koncentrácie substrátu zvyšuje rýchlosť len do určitej miery a ďalej nie je možné ju zvýšiť pridávaním substrátu. Nemecký biochemik Leonor Michaelis a kanadská lekárka Maud Mentenová odvodili vzťah medzi rýchlosťou enzýmovej reakcie a koncentráciou substrátu, ktorý je po nich pomenovaný Michaelis–Mentenovej rovnica:
- v - rýchlosť enzýmovej reakcie
- Vmax - maximálna rýchlosť enzýmovej reakcie
- [S] - koncentrácia substrátu
- KM - Michaelisova konštanta
Externé odkazy
- Názvoslovie enzýmov (en)
- BRENDA (en)
Šablóna:Link FA Šablóna:Link FA Šablóna:Link FA Šablóna:Link FA



![{\displaystyle [P]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/25d78ad4ad13872df07ac9b02a2574250a0e54fd)
![{\displaystyle [ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/31639ab6b9c7c728139b5f8ce03991d800ac7741)
![{\displaystyle v={\frac {V_{max}[S]}{K_{M}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e8f4ef73642e1744b8816d74c408901b8a0e16d1)