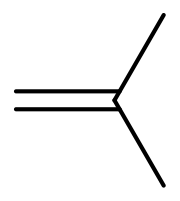
Izobutén
| Izobutén | |||||||||||||||||||
 | |||||||||||||||||||
 | |||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||
| Sumárny vzorec | C4H8 | ||||||||||||||||||
| Systematický názov | 2-metylpropén | ||||||||||||||||||
| Vzhľad | bezfarebný plyn | ||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||
| Molárna hmotnosť | 56,106 g/mol | ||||||||||||||||||
| Teplota topenia | −140,3 °C (132,8 K)[1] | ||||||||||||||||||
| Teplota varu | −6,9 °C (266,2 K)[1] | ||||||||||||||||||
| Hustota | 0,5879 g/cm3, kvapalina pri 25 °C[1] | ||||||||||||||||||
| Rozpustnosť | nerozpustný vo vode | ||||||||||||||||||
| |||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||
| Číslo CAS | 115-11-7 | ||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||
Izobutén, triviálny názov izobutylén, je uhľovodík so štyrmi atómami uhlíka. Je to vetvený alkén a je to jeden zo štyroch izomérov buténu. Je to bezfarebný horľavý plyn, ktorý je významný v priemysle.[1]
Výroba
[upraviť | upraviť zdroj]Izobutén je najreaktívnejším izomérom buténu, čo sa využíva pri jeho separácii od ostatných buténov. Izobutén sa prevedie na nejaký derivát (typicky hydratáciou), vyseparuje od zmesi buténov a potom sa prevedia naspäť na izobutén pre ďalšie použitie.[1]
Izobutylén vysokej kvality sa zvyčajne získava dehydratáciou terc-butanolu (t-BuOH) alebo katalytickou dehydrogenáciou izobutánu (pomocou procesu Catofin alebo jemu podobných).[1][2]
Izobutylén je vedľajší produkt eténolýzy diizobutylénu, ktorou vzniká neohexén:[3]
- (CH3)3C-CH=C(CH3)2 + CH2=CH2 → (CH3)3C-CH=CH2 + (CH3)2C=CH2
Metylterc-butyléter (MTBE) a etylterc-butyléter (ETBE), ktoré sa pridávajú do benzínu, sa vyrábajú z metanolu a etanolu reakciou s izobuténom, a to buď priamo (s izobuténom pochádzajúcim z dehydratácie t-BuOH), alebo v prúde buténov pochádzajúcom z rafinérie. Izobutén sa v týchto prúdoch zvyčajne od ostatných alkénov pred reakciou neseparuje, pretože je jednoduchšie od seba oddeliť étery od ostatných buténov až po reakcii.[1] Veľmi čistý izobutén je možné získať i zahriatím MTBE na vysokú teplotu a následnou destiláciou z metanolu.[4]
Použitie
[upraviť | upraviť zdroj]Izobutén sa používa pri výrobe rôznych produktov. Izooktán, prídavok do paliva, vzniká alkyláciou izobuténu[1] s butánom alebo dimerizáciou izobuténu, ktorou vzniká diizobutylén, ktorý sa potom hydrogenuje za vzniku izooktánu.[5] Izobutén sa využíva i pri výrobe metakrylaldehydu a kyseliny metakrylovej.[1] Izobutén sa používa i na výrobu izoprénu.[6] Polymerizáciou izobuténu vzniká polyizobutylén alebo pri kopolymerizácii s izoprénom vzniká butylkaučuk.[1] Friedel-Craftsovou alkyláciou fenolov s izobutylénom vznikajú antioxidanty,[1] ako sú butylovaný hydroxytoluén a butylovaný hydroxyanizol.
terc-butylamín sa komerčne vyrába amináciou izobutylénu s využitím zeolitových katalyzátorov:[7]
- NH3 + CH2=C(CH3)2 → H2NC(CH3)3
Z izobuténu sa vyrába i terc-butanol, ktorý sa používa ako rozpúšťadlo.[8] Reakciou terc-butanolu s kovovým draslíkom vzniká terc-butoxid draselný,[9] ktorý sa používa ako silná nenukleofilná báza v organickej syntéze.[10]
Bezpečnosť
[upraviť | upraviť zdroj]Izobutén je veľmi horľavý plyn.[1]
Referencie
[upraviť | upraviť zdroj]- ↑ a b c d e f g h i j k l GEILEN, Frank M.A.; STOCHNIOL, Guido; PEITZ, Stephan. Butenes. Weinheim, Germany : Wiley-VCH Verlag GmbH & Co. KGaA, 2014-01-31. DOI: 10.1002/14356007.a04_483.pub3. Dostupné online. ISBN 978-3-527-30673-2. DOI:10.1002/14356007.a04_483.pub3 S. 1–13. (po anglicky)
- ↑ OLAH, George A.. Hydrocarbon chemistry. Hoboken, N.J. : [s.n.], 2003. (2nd edition.) Dostupné online. ISBN 0-471-41782-3.
- ↑ DELAUDE, Lionel; NOELS, Alfred F. Kirk-Othmer Encyclopedia of Chemical Technology. [s.l.] : Wiley. Kapitola Metathesis.
- ↑ MEUNIER, P. B.; CHAUMETTE, P.. Production d'isobutène de haute pureté par décomposition du MTBE. Revue de l'Institut Français du Pétrole, 1991-05-01, roč. 46, čís. 3, s. 361–387. Dostupné online [cit. 2022-09-28]. ISSN 0020-2274. DOI: 10.2516/ogst:1991017. (po francúzsky)
- ↑ GOORTANI, Behnam M.; GAURAV, Aashish; DESHPANDE, Alisha. Production of Isooctane from Isobutene: Energy Integration and Carbon Dioxide Abatement via Catalytic Distillation. Industrial & Engineering Chemistry Research, 2015-04-15, roč. 54, čís. 14, s. 3570–3581. Dostupné online [cit. 2022-09-28]. ISSN 0888-5885. DOI: 10.1021/ie5032056. (po anglicky)
- ↑ izoprén. In: BÍNA, Jaroslav. Malá encyklopédia chémie. Bratislava : Obzor, 1981. S. 349.
- ↑ ELLER, Karsten; HENKES, Erhard; ROSSBACHER, Roland. Amines, Aliphatic. Weinheim, Germany : Wiley-VCH Verlag GmbH & Co. KGaA, 2000-06-15. DOI: 10.1002/14356007.a02_001. Dostupné online. ISBN 978-3-527-30673-2. DOI:10.1002/14356007.a02_001 S. a02_001. (po anglicky)
- ↑ butanoly. In: BÍNA, Jaroslav. Malá encyklopédia chémie. Bratislava : Obzor, 1981. S. 154.
- ↑ Organic Syntheses Procedure [online]. www.orgsyn.org, [cit. 2022-09-28]. Dostupné online. (po anglicky)
- ↑ CAINE, Drury. Potassium tert -Butoxide. Chichester, UK : John Wiley & Sons, Ltd, 2006-09-15. DOI: 10.1002/047084289X.rp198.pub2. Dostupné online. ISBN 978-0-471-93623-7. DOI:10.1002/047084289x.rp198.pub2 S. rp198.pub2. (po anglicky)
Zdroj
[upraviť | upraviť zdroj]Tento článok je čiastočný alebo úplný preklad článku Isobutylene na anglickej Wikipédii.



