Tymolftaleín: Rozdiel medzi revíziami
typografia |
kategórie, typografia |
||
| Riadok 1: | Riadok 1: | ||
{{Infobox Chemická zlúčenina|Názov=Tymolftaleín|Vzorec=C<sub>28</sub>H<sub>30</sub>O<sub>4</sub>|Vzhľad=bezfarebná tuhá látka|Teplota topenia=252 °C|Obrázok=Thymolphthalein.svg|Anglický názov=Thymolphtalein|NFPA 704={{NFPA 704 |Horľavosť = 0 |Zdravie = 1 |Reaktivita = 0 |Ostatné = }}|GHS piktogram={{GHS|08}}}} |
{{Infobox Chemická zlúčenina|Názov=Tymolftaleín|Vzorec=C<sub>28</sub>H<sub>30</sub>O<sub>4</sub>|Vzhľad=bezfarebná tuhá látka|Teplota topenia=252 °C|Obrázok=Thymolphthalein.svg|Anglický názov=Thymolphtalein|NFPA 704={{NFPA 704 |Horľavosť = 0 |Zdravie = 1 |Reaktivita = 0 |Ostatné = }}|GHS piktogram={{GHS|08}}}} |
||
'''Tymolftaleín''' je bázický [[Indikátor (chémia)|indikátor]] (reaguje na [[Zásada (chémia)|zásady]]). V pevnom skupenstve má podobu bezfarebného prášku. V zásadách sa sfarbuje do tmavomodra. Tymolftaleín sa donedávna používal, ako preháňadlo. V dnešnej dobe sa od tohto využitia ustupuje. Tymolftaleín má zrejme [[Karcinogén|karcinogénne]] účinky. Od [[Kyslosť|pH]] 9,4 |
'''Tymolftaleín''' je bázický [[Indikátor (chémia)|indikátor]] (reaguje na [[Zásada (chémia)|zásady]]). V pevnom skupenstve má podobu bezfarebného prášku. V zásadách sa sfarbuje do tmavomodra. Tymolftaleín sa donedávna používal, ako preháňadlo. V dnešnej dobe sa od tohto využitia ustupuje. Tymolftaleín má zrejme [[Karcinogén|karcinogénne]] účinky. Od [[Kyslosť|pH]] 9,4{{--}}10,5 mení svoj bezfarebný stav na modrý. |
||
== Využitie == |
== Využitie == |
||
{{PH indikátor|názov=Tymolftaleín|dolné pH=9,3|dolné pH farba=white|horné pH=10,5|horné pH farba=blue|horné pH text=white}} |
{{PH indikátor|názov=Tymolftaleín|dolné pH=9,3|dolné pH farba=white|horné pH=10,5|horné pH farba=blue|horné pH text=white}} |
||
V |
V chémii sa tymolftaleín využíva pri [[Titrácia|acidobázických titráciach]]. Nie je síce využívaný tak často, ako [[fenolftaleín]], ale používa sa najmä pre jeho výrazné farebné zmeny. |
||
== Príklad == |
== Príklad == |
||
| Riadok 12: | Riadok 12: | ||
== Pozri aj == |
== Pozri aj == |
||
* [[Indikátor (chémia)]] |
* [[Indikátor (chémia)]] |
||
* [[Fenolftaleín]] |
* [[Fenolftaleín]] |
||
* [[Lakmus]] |
* [[Lakmus]] |
||
| Riadok 19: | Riadok 18: | ||
* [[Fuksín]] |
* [[Fuksín]] |
||
* [[Indigokarmín]] |
* [[Indigokarmín]] |
||
[[Kategória:Acidobázické indikátory]] |
|||
[[Kategória:Laktóny]] |
|||
Verzia z 13:08, 15. január 2017
| Tymolftaleín | |||||||||||||
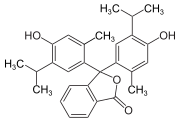 | |||||||||||||
| Všeobecné vlastnosti | |||||||||||||
| Sumárny vzorec | C28H30O4 | ||||||||||||
| Vzhľad | bezfarebná tuhá látka | ||||||||||||
| Fyzikálne vlastnosti | |||||||||||||
| Teplota topenia | 252 °C | ||||||||||||
| |||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||
Tymolftaleín je bázický indikátor (reaguje na zásady). V pevnom skupenstve má podobu bezfarebného prášku. V zásadách sa sfarbuje do tmavomodra. Tymolftaleín sa donedávna používal, ako preháňadlo. V dnešnej dobe sa od tohto využitia ustupuje. Tymolftaleín má zrejme karcinogénne účinky. Od pH 9,4 – 10,5 mení svoj bezfarebný stav na modrý.
Využitie
| Tymolftaleín (indikátor) | ||
| pod pH 9,3 | nad pH 10,5 | |
| 9,3 | ↔ | 10,5 |
V chémii sa tymolftaleín využíva pri acidobázických titráciach. Nie je síce využívaný tak často, ako fenolftaleín, ale používa sa najmä pre jeho výrazné farebné zmeny.
Príklad
V kadičke je roztok kyseliny uhličitej (H2CO3) a tymolftaleínu (roztok je bezfarebný). Postupne začneme byretou do kadičky prilievať vodný roztok hydroxidu sodného (NaOH). Keď sa roztok v kadičke sfarbí namodro, určíme bod ekvivalencie titrácie.


