Kyselina peroxodisírová: Rozdiel medzi revíziami
Menšie opravy |
Bez shrnutí editace |
||
| Riadok 52: | Riadok 52: | ||
}} |
}} |
||
'''Kyselina peroxodisírová''' H<sub>2</sub>S<sub>2</sub>O<sub>8</sub>, tiež sa nazýva '''Marshallová kyselina''' po profesorovi [[Hugh Marshall|Hughovi Marshallovi]], ktorý ju ako prvý vytvoril, je |
'''Kyselina peroxodisírová''' H<sub>2</sub>S<sub>2</sub>O<sub>8</sub>, tiež sa nazýva '''Marshallová kyselina''' po profesorovi [[Hugh Marshall|Hughovi Marshallovi]], ktorý ju ako prvý vytvoril, je jednou z [[Peroxokyselina|peroxokyselín]] [[Síra|síry]]. [[Anión]] vznikajúci nahradením dvoch atómov [[vodík]]a sa nazýva ''peroxodisíranový'' (zastaralo ''persíranový anión''). Soli odvodené od kyseliny peroxodisírovej sa nazývajú [[peroxosírany|peroxodisírany]] a [[hydrogenperoxodisírany]]. |
||
== Vlastnosti == |
== Vlastnosti == |
||
| Riadok 71: | Riadok 71: | ||
== Použitie == |
== Použitie == |
||
Kyselina peroxodisírová sa používa na výrobu farbív a [[Peroxid vodíka|peroxidu vodíka]]. Využíva sa aj v [[Analytická chémia|analytickej chémii]]. |
Kyselina peroxodisírová sa používa na výrobu farbív a [[Peroxid vodíka|peroxidu vodíka]]. Využíva sa aj v [[Analytická chémia|analytickej chémii]]. |
||
== Literatúra == |
== Literatúra == |
||
{{Citácia knihy|priezvisko=Greenwood|meno=Norman Neill|titul=Chemie prvků|vydanie=1|vydavateľ=Informatorium|miesto=Praha|rok=1993|isbn=80-85427-38-9|priezvisko2=Earnshaw|meno2=Alan|jazyk=po česky}} |
*{{Citácia knihy|priezvisko=Greenwood|meno=Norman Neill|titul=Chemie prvků|vydanie=1|vydavateľ=Informatorium|miesto=Praha|rok=1993|isbn=80-85427-38-9|priezvisko2=Earnshaw|meno2=Alan|jazyk=po česky}} |
||
== Referencie == |
== Referencie == |
||
| Riadok 81: | Riadok 79: | ||
== Iný projekt == |
== Iný projekt == |
||
{{Projekt |
{{Projekt}} |
||
== Zdroj == |
== Zdroj == |
||
Verzia z 20:11, 19. marec 2021
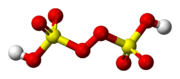
| Kyselina peroxodisírová | |||||||||||||||||||
 | |||||||||||||||||||
 | |||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||
| Sumárny vzorec | H2S2O8 (S02OH)2OO | ||||||||||||||||||
| Synonymá | Sulfooxyhydrogénsulfát (IUPAC) Kyselina perdisírová Kyselina peroxydisírová Marshallová kyselina | ||||||||||||||||||
| Vzhľad | Nestabilná bezfarebná kryštalická látka | ||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||
| Molekulová hmotnosť | 194,1 u | ||||||||||||||||||
| Molárna hmotnosť | 194,1411 g/mol | ||||||||||||||||||
| Teplota rozkladu | 65 °C | ||||||||||||||||||
| Hustota | 2,5 ± 0,1 g/cm3 | ||||||||||||||||||
| |||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||
| Číslo CAS | 13445-49-3 | ||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||
Kyselina peroxodisírová H2S2O8, tiež sa nazýva Marshallová kyselina po profesorovi Hughovi Marshallovi, ktorý ju ako prvý vytvoril, je jednou z peroxokyselín síry. Anión vznikajúci nahradením dvoch atómov vodíka sa nazýva peroxodisíranový (zastaralo persíranový anión). Soli odvodené od kyseliny peroxodisírovej sa nazývajú peroxodisírany a hydrogenperoxodisírany.
Vlastnosti
Kyselina peroxodisírová je nestabilná bezfarebná kryštalická látka so silnými oxidačnými účinkami. Reaguje až výbušne s organickými látkami.
Syntéza
Kyselina peroxodisírová sa pripravuje reakciou kyseliny chlórsírovej s peroxidom vodíka:[1]
- 2ClSO3H + H2O2 → H2S2O8 + 2 HCl
Ďalšou metódou je elektrolýza mierne koncentrovanej kyseliny sírovej (60 - 70%) s platinovými elektródami pri vysokej prúdovej hustote a napätí:
- H2SO4 + H2O → H3O+ + HSO4− (disociácia kyseliny sírovej)
- 2HSO4− → H2S2O8 + 2e− (E0 = +2.4V) (oxidácia hydrogénsíranu)
- 2H2SO4 → H2S2O8 + H2 (celková reakcia)
- 3H2O → O3 + 6H+ (ozón ako vedľajší produkt)
Použitie
Kyselina peroxodisírová sa používa na výrobu farbív a peroxidu vodíka. Využíva sa aj v analytickej chémii.
Literatúra
- GREENWOOD, Norman Neill; EARNSHAW, Alan. Chemie prvků. 1. vyd. Praha : Informatorium, 1993. ISBN 80-85427-38-9. (po česky)
Referencie
- ↑ JAKOB, Harald; LEININGER, Stefan; LEHMANN, Thomas, et al. "Peroxo Compounds, Inorganic". Weinheim: Wiley-VCH, 2007-07-15, [cit. 2021-03-19]. DOI:10.1002/14356007.a19_177.pub2 (po anglicky)
Iný projekt
 Commons ponúka multimediálne súbory na tému Kyselina peroxodisírová
Commons ponúka multimediálne súbory na tému Kyselina peroxodisírová
Zdroj
Tento článok je čiastočný alebo úplný preklad článkov Kyselina peroxodisírová na českej Wikipédii a Peroxydisulfuric acid na anglickej Wikipédii.

