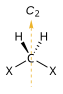Chiralita (chémia)
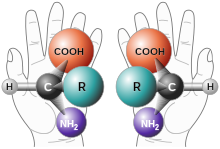
V chémii sa molekula nazýva chirálnou, pokiaľ nie je možné ju zjednotiť s jej zrkadlovým obrazom žiadnou kombináciou rotácií, translácií alebo nejakými konformačnými zmenami. Táto geometrická vlastnosť sa označuje ako chiralita.[1][2][3][4][5] Tento pojem pochádza zo starogréckeho είρ (cheir), „ruka“, čo je bežný príklad objektu s touto vlastnosťou.
Chirálna molekula existuje v podobe dvoch stereoizomérov, ktoré sú vzájomne zrkadlovými obrazmi. Tieto stereoizoméry sa nazývajú enantioméry – často sa rozlišujú ako „pravotočivý“ alebo „ľavotočivý“ podľa ich absolútnej konfigurácie alebo iného kritéria. Dva enantioméry majú rovnaké chemické vlastnosti, okrem ich reaktivity s inými chirálnymi zlúčeninami. Majú zároveň i zhodné fyzikálne vlastnosti, okrem toho, že majú často opačnú optickú aktivitu. Optická aktivita enantiomérov však môže byť veľmi nízka, čo sa potom označuje ako kryptochiralita. Homogénna zmes dvoch enantiomérov v rovnakom pomere sa nazýva racemát a zvyčajne sa líši (chemicky i fyzikálne) od čistých enantiomérov.

Chirálne molekuly majú zvyčajne stereogénny prvok, na základe ktorého chiralita vzniká. Najbežnejší typ stereogénneho prvku je stereogénne centrum (stereocentrum). V prípade organických zlúčenín sú to typicky uhlíkové atómy, na ktorých sú v tetraédrickej geometrii naviazané štyri rôzne skupiny. Pre dané stereocentrum sú dva spôsoby, ktorými je možné tieto skupiny naviazať, čím vznikajú stereoizoméry (diastereoméry a enantioméry) u molekúl s viac než jedným stereocentrom. U chirálnych molekúl s jedným alebo viacerými stereocentrami odpovedá enantioméru ten stereoizomér, v ktorom majú všetky stereocentrá opačnú konfiguráciu. Inak povedané, pre konkrétnu molekulu má pár enantiomérov opačné konfigurácie na všetkých stereocentrách. Organická zlúčenina, ktorá má len jeden stereogénny uhlík, je vždy chirálna. Oproti tomu sú zlúčeniny, ktoré majú viac stereogénnych uhlíkov, zvyčajne ale nie vždy chirálne. Totiž, ak sú stereocentrá usporiadané tak, že molekula má vnútornú rovinu symetrie, tak je molekula achirálna a označuje sa ako mezozlúčenina. Ostatné atómy, napríklad N, P, S alebo Si, môžu byť takisto stereocentrami, ak sú na nich naviazané štyri rôzne substituenty (vrátane voľného elektrónového páru).
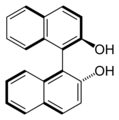
Molekuly, ktorých chiralita pochádza z prítomnosti jedného alebo viacerých stereocentier, majú centrálnu chiralitu. Existujú ešte dva druhy stereogénnych prvkov, ktoré môžu viesť k chiralite: stereogénna os (axiálna chiralita) a stereogénna rovina (planárna chiralita). Posledným spôsobom, ktorým môže byť molekula chirálna, je kvôli jej prirodzenému zakriveniu v priestore (inherentná chiralita). Tieto druhy chirality sú však omnoho menej časté, než centrálna chiralita. BINOL je typický príklad axiálne chirálnej molekuly a trans-cyklooktén je bežný príklad planárne chirálnej molekuly. Helicén má helikálnu chiralitu, čo je jeden z druhov inherentnej chirality.
-
(R) enantiomér BINOLu, príklad axiálnej chirality.
-
Dva enantioméry trans-cyklookténu, príklad planárnej chirality.
-
10-Helicén, ktorý má helikálnu štruktúru a teda je inherentne chirálny.
Chiralita je dôležitý koncept v stereochémii a biochémii. Väčšina zlúčenín, ktoré sú dôležité v biológii, je chirálna, napríklad sacharidy (cukry, škrob a celulóza), aminokyseliny, z ktorých sa skladajú bielkoviny, a nukleové kyseliny. V živých organizmoch sa typicky nachádza len jeden z dvoch enantiomérov chirálnej zlúčeniny. Z tohto dôvodu vedia organizmy, ktoré prijímajú chirálne zlúčeniny, spracovať zvyčajne len jeden z jeho enantiomérov. Z toho istého dôvodu majú dva enantioméry chirálneho liečiva veľmi rozdielne účinky alebo silu.
Chiralita je vnútorná vlastnosť identity molekuly, takže systematický názov musí zahŕňať detaily jej absolútnej konfigurácie (R/S, D/L alebo iné deskriptory).
Definícia[upraviť | upraviť zdroj]
Chiralita molekuly je daná molekulárnou symetriou a jej konformáciami. Konformácia molekuly je chirálna len vtedy, keď patrí do bodových grúp Cn, Dn, T, O alebo I (chirálne bodové grupy). To, či je daná molekula považovaná za chirálnu však záleží na tom, či je možné jej chirálne konformácie izolovať ako separovateľné enantioméry, aspoň teoreticky, alebo či sa tieto enantiomérne konforméry rýchlo menia z jedného na druhý pri danej teplote a v krátkych časových intervaloch vďaka nízkoenergetickým konformačným zmenám (čím sa molekula stáva achirálnou). Napríklad bután sa pri izbovej teplote považuje za achirálny, aj keď jeho gauche izomér (dihedrálny uhol definovaný štyrmi uhlíkovými atómami má hodnotu približne 60°) nie je identický s jeho zrkadlovým obrazom, pretože rotácia okolo stredovej C–C väzby je príliš rýchla, čím dochádza k premene jedného enantioméru na druhý (energetická bariéra 3,4 kcal/mol) a teda enantioméry nie je možné separovať. Podobným spôsobom sa cis-1,2-dichlórhexán nachádza v stoličkových konformáciách, ktoré sú nezjednotiteľné zrkadlové obrazy, ale jeden sa môže meniť na druhý (energetická bariéra ~10 kcal/mol). Ako ďalší príklad, amíny s tromi rôznymi substituentmi (R1R2R3N:) sú takisto považované za achirálne molekuly, pretože enantiomérna pyramídová konformácia sa rýchlo mení z jednej strany na druhú preklápaním cez planárny tranzitný stav, čím dochádza k premene jedného enantioméru na druhý (energetická bariéra ~6 kcal/mol). Ak je však teplota dostatočne nízka, je premena jedného enantioméru na druhý, kvôli ktorej sú tieto molekuly achirálne pri izbovej teplote, príliš pomalá v danom časovom intervale (zvyčajne sa 1000 sekúnd považuje za vhodný časový interval kvôli chemickej alebo chromatografickej separácii enantiomérov), vďaka čomu sa tieto molekuly stávajú chirálnymi pri nízkych teplotách. Molekuly, ktoré sú chirálne pri izbovej teplote kvôli nepovolenej rotácii okolo jednoduchej väzby (bariéra rotácie ≥ asi 23 kcal/mol) sú takzvane atropoizomérne.
Chirálne zlúčeniny nemôžu obsahovať nevlastnú os (Sn), ktorá sa skladá z osi symetrie a roviny symetrie kolmej na os.[6] Chirálne molekuly sú vždy nesymetrické (bez Sn), ale nie vždy asymetrické (bez akýchkoľvek prvkov symetrie okrem triválnej identity). Asymetrické molekuly sú vždy chirálne.[7]
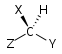
Nasledujúca tabuľka ukazuje príklady chirálnych a achirálnych molekúl so Schoenfliesovou notáciou bodovej grupy molekuly. U achirálnych molekúl reprezentujú X a Y (bez označenia) achirálne skupiny, zatiaľ čo XR/XS a YR/YS reprezentujú enantioméry. Na orientácii S2 osi nezáleží, pretože ide len o inverziu. Akákoľvek orientácia tejto osi je vhodná, ak prechádza stredom inverzie. Existujú aj vyššie symetrie chirálnach a achirálnych molekúl a takisto existujú symetrie iné než tie uvedené v tabuľke, napríklad chirálne C3 a achirálne S4.
Stereogénne centrá[upraviť | upraviť zdroj]
Mnohé chirálne molekuly majú bodovú chiralitu, teda majú jedno chirálne stereocentrum, ktoré je zhodné s niektorým z atómov. Toto stereogénne centrum má zvyčajne štyri alebo viac väzieb na rôzne skupiny a môže to byť uhlík (ako je to vo väčšine biologických molekúl), fosfor (ako je to u organofosfátov), kremík alebo atóm kovu (ako v mnohých chirálnych koordinačných zlúčeninách). Stereogénne centrum môže byť aj trojväzbový atóm, ak jeho väzby nie sú v tej istej rovine, napríklad fosfor v P-chirálnych fosfínoch (PRR′R″) a síra v S-chirálnych sulfoxidoch (OSRR′), pretože namiesto štvrtej väzby obahujú voľný elektrónový pár.
Chiralita môže vznikať i na základe rôznych izotopov, ako napríklad u deuterovaného benzylalkoholu PhCHDOH, ktorý je chirálny a opticky aktívny ([α]D = 0.715°), aj keď nedeuterovaný PhCH2OH nie je.[8]
Ak sa dva enantioméry ľahko menia jeden na druhý, môže byť prakticky nemožné tieto enantioméry separovať, takže je pozorovateľný len racemát. Tak je to napríklad u väčšiny amínov s troma rôznymi substituentami (NRR′R″), kvôli nízkej energetickej bariére inverzie dusíka.
Dôsledky chirality[upraviť | upraviť zdroj]
Chiralita sa prejavuje rôznymi spôsobmi:
- Chuť: Umelé sladidlo aspartám má dva enantioméry. L-Aspartám je sladký, zatiaľ čo D-aspartám je bez chuti.[9]
- Vôňa: (R)-Karvón vonia ako mäta, zatiaľ čo (S)-karvón vonia ako rasca.[10]
- Účinnosť liekov: Antidepresívum Citalopram sa predáva ako racemát. Štúdie však preukázali, že (S) enantiomér je zodpovedný za účinok tohto lieku.[11][12] Tento enantiomér sa označuje ako Escitalopram a je možné ho kúpiť i samostatne.[13]
- Bezpečnosť liekov: D-Penicilamín sa používa v rámci chelačnej terapie a na liečbu reumatoidnej artritídy, zatiaľ čo L-penicilamín je toxický a inhibuje pôsobenie pyridoxínu, esenciálneho B vitamínu.[14]
V biochémii[upraviť | upraviť zdroj]
Mnoho biologicky aktívnych zlúčenín je chirálnych, vrátane prírodných aminokyselín (stavebných blokov bielkovín) a sacharidov.
Pôvod prítomnosti enantiomérne čistých látok v biológii je téma mnohých debát.[15] Väčšina vedcov verí, že „výber“ chirality v živote na Zemi bol náhodný a keby život založený na uhlíku existoval kdekoľvek inde vo vesmíre, teoreticky by mohol mať opačnú chiralitu. Rané aminokyseliny sa však mohli vytvoriť v prachu komét. V tomto prípade mohla cirkulárne polarizovaná radiácia (ktorá tvorí 17 % hviezdnej radiácie) selektívne zničiť aminokyseliny jednej chirality, čo by viedlo k výberu konkrétnej chirality a malo za následok entatiomérnu čistotu všetkého života na zemi.[16][17]
Enzýmy, ktoré sú chirálne, často rozlišujú medzi dvoma enantiomérmi chirálneho substrátu. Dá sa povedať, že enzým má dutinu podobnú rukavici, ktorá viaže substrát. Ak je to rukavica na pravú ruku, tak jeden enantiomér sa zmestí dovnútra a bude sa viazať, ale druhý enantiomér sa do nej nezmestí a pravdepodobne sa viazať nebude.
Aminokyseliny v L konfigurácii sú zvyčajne bez chuti, zatiaľ čo D-aminokyseliny zvyknú chutiť sladko.[15] Listy mäty obsahujú (R)-karvón a semienka rasce obsahujú (S)-karvón.[18] Každá táto látka vonia väčšine ľudí inak, pretože receptory vône sú chirálne.
Chiralita je dôležitá i v kontexte usporiadaných fáz. Pridaním malého množstva opticky aktívnej molekuly do nematickej fázy (fázy, ktorá má molekuly zoradené podľa nejakej polárnej orientácie) sa táto váza premení na chirálnu nematickú fázu (cholesterickú fázu). Chiralita v tomto kontexte u polymérnych tekutín bola takisto študovaná.[19]
V organickej chémii[upraviť | upraviť zdroj]

Chiralita je vlastnosť symetrie, nie vlastnosť ktorejkoľvek časti periodickej tabuľky. Mnoho organických materiálov, molekúl a iónov je teda chirálnych. Kremeň je jedným z príkladov zo sveta minerálov. Takéto necentrické materiály sú zaujímavé hlavne pre aplikácie v nelineárnej optike.
V prípade koordinačnej a organokovovej chémie je chiralita často pozorovaná a má svoj význam. Známou zlúčeninou je tris(bipyridín)ruténatý komplex, v ktorom majú tri bipyridínové ligandy tvar chirálnej vrtule.[20] Dva enantioméry komplexov ako je [Ru(2,2′-bipyridín)3]2+ sa označujú ako Λ (veľká lambda, grécke písmeno ekvivalentné „L“) pre ľavotočivý variant a Δ (veľká delta, grécke písmeno ekvivalentné „D“) pre pravotočivý variant (na obrázku vpravo).
Chirálne ligandy spôsobujú chiralitu komplexov kovov, ako je to u komplexov kovov s aminokyselinami. Ak má kov katalytické vlastnosti, jeho kombinácia s chirálnymi ligandmi je základom asymetrickej katalýzy.[21]
Metódy a využitie[upraviť | upraviť zdroj]
Pojem optická aktivita je odvodený od interakcie chirálnych materiálov s polarizovaným svetlom. V roztoku spôsobuje (−)-forma optického izoméru otočenie roviny lúča lineárne polarizovaného svetla proti smeru hodinových ručičiek. Naopak (+)-forma robí presne opačnú vec a stáča ho v smere hodinových ručičiek. Na meranie zmeny roviny polarizovaného svetla sa používa polarimeter a táto zmena sa vyjadruje ako optická rotácia.
Enantioméry je možné rozdeliť chirálnymi metódami. Tie často spočívajú v tvorbe kryštálov solí tvorených jedným z enantiomérov a kyseliny alebo zásady z chirálnych látok vyskytujúcich sa v prírode, napríklad kyseliny jablčnej alebo amínu brucínu. Niektoré racemáty spontánne kryštalizujú do pravotočivých a ľavotočivých kryštálov, ktoré sa dajú oddeliť rukou. Louis Pasteur použil túto metódu na separáciu kryštálov ľavotočivého a pravotočivého vínanu sodno-amónneho v roku 1849. Niekedy je možné túto kryštalizáciu „spustiť“ pomocou ľavo- alebo pravotočivého kryštálu, aby každý z týchto kryštálov narástol.
Názvoslovie spojené s chiralitou[upraviť | upraviť zdroj]
- „Racemická zmes“ (zmes opačných enantiomérov v pomere 1:1) by sa správne mala označovať ako racemát alebo racemický konglomerát[22]
- Neracemické chirálne zmesi sa niekedy nazývajú skalemické, odporúča sa však označovať ich ako enantiomérne obohatené (ak je väčšina tvorená jedným enantiomérom),[22][23] prípadne enantiomérne čisté[22][24]
- Látky, ktoré obsahujú len jeden enantiomér, sa nazývajú enantiomérne čisté.[25] Niekedy sa označujú i ako homochirálne, ale toto označenie sa už neodporúča používať.[25][26]
- Enantiomérny nadbytok (% ee) označuje rozdiel, o koľko viac je jedného enantioméru oproti druhému. Napríklad vzorka so 40% e.e. R-enantioméru obsahuje 70 % R a 30 % S (70 % - 30 % = 40 %)[27]
História[upraviť | upraviť zdroj]
Rotácia roviny polarizovaného svetla chirálnymi látkami bola prvýkrát pozorovaná Jean-Baptistie Biotom v roku 1812[28] a následne sa stala dôležitou v priemysle spracovania cukru, analytickej chémii a farmaceutickom priemysle. Louis Pasteur v roku 1848 usúdil, že tento fenomén má molekulárny základ.[29][30] Názov „chiralita“ prvýkrát použil Lord Kelvin v roku 1894.[31] Rôzne enantioméry alebo diastereoméry zlúčenín sa označovali ako optické izoméry kvôli ich rozdielnym optickým vlastnostiam.[32] V jednom momente sa predpokladalo, že chiralita existuje len v organickej chémii, ale táto mylná predstava sa zmenila preukázaním štruktúry čisto anorganickej zlúčeniny, komplexu kobaltu známeho ako hexol, ktorú ukázal Alfred Werner v roku 1911.[33]
Na začiatku 70. rokoch 20. storočia ukázali rôzne vedecké skupiny, že ľudský čuchový orgán je schopný rozlíšiť chirálne zlúčeniny.[10][34][35]
Referencie[upraviť | upraviť zdroj]
- ↑ MORAVČÍK, Jakub; HROBOŇOVÁ, Katarína. Separácia enantiomérov aminokyselín metódou vysokoúčinnej kvapalinovej chromatografie [online]. www.prolekare.cz, [cit. 2022-04-09]. Dostupné online.
- ↑ Organic Chemistry (4th Edition) Paula Y. Bruice. Pearson Educational Books. ISBN 9780131407480
- ↑ Organic Chemistry (3rd Edition) Marye Anne Fox, James K. Whitesell Jones & Bartlett Publishers (2004) ISBN 0763721972
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Chirality". DOI:10.1351/goldbook.C01058
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Superposability". DOI:10.1351/goldbook.S06144
- ↑ Symetrie molekul [online]. is.muni.cz, [cit. 2022-04-09]. Dostupné online.
- ↑ Cotton, F. A., "Chemical Applications of Group Theory," John Wiley & Sons: New York, 1990.
- ↑ ↑ Stereochemistry of the Primary Carbon. X. Stereochemical Configurations of Some Optically Active Deuterium Compounds. Tetrahedron, 1959, s. 338–344. DOI: 10.1016/0040-4020(59)80014-4.
- ↑ GAL, Joseph. The Discovery of Stereoselectivity at Biological Receptors: Arnaldo Piutti and the Taste of the Asparagine Enantiomers-History and Analysis on the 125th Anniversary. Chirality, 2012, s. 959–976. DOI: 10.1002/chir.22071. PMID 23034823.
- ↑ a b Chemical and sensory data supporting the difference between the odors of the enantiomeric carvones. J. Agric. Food Chem., 1971, s. 785–787. DOI: 10.1021/jf60176a035.
- ↑ Do equivalent doses of escitalopram and citalopram have similar efficacy? A pooled analysis of two positive placebo-controlled studies in major depressive disorder. Int Clin Psychopharmacol, May 2004, s. 149–55. DOI: 10.1097/00004850-200405000-00005. PMID 15107657.
- ↑ HYTTEL, J.; Bøgesø, K. P.; Perregaard, J.. The pharmacological effect of citalopram resides in the (S)-(+)-enantiomer. Journal of Neural Transmission, 1992, s. 157–160. DOI: 10.1007/BF01244820. PMID 1632943.
- ↑ Escitalopram Monograph for Professionals [online]. Drugs.com, [cit. 2022-04-09]. Dostupné online. (po anglicky)
- ↑ JAFFE, IA; ALTMAN, K; MERRYMAN, P. The Antipyridoxine Effect of Penicillamine in Man.. The Journal of Clinical Investigation, Oct 1964, s. 1869–73. DOI: 10.1172/JCI105060. PMID 14236210.
- ↑ a b Meierhenrich, Uwe J.. Amino acids and the Asymmetry of Life. Berlin, GER : Springer, 2008. ISBN 978-3540768852.
- ↑ MCKEE, Maggie. Space radiation may select amino acids for life [online]. New Scientist, [cit. 2016-02-05]. Dostupné online. (po anglicky)
- ↑ Meierhenrich Uwe J., Nahon Laurent, Alcaraz Christian, Hendrik Bredehöft Jan, Hoffmann Søren V., Barbier Bernard, Brack André. Asymmetric Vacuum UV photolysis of the Amino Acid Leucine in the Solid State. Angew. Chem. Int. Ed., 2005, s. 5630–5634. DOI: 10.1002/anie.200501311. PMID 16035020.
- ↑ Chemical and sensory data supporting the difference between the odors of the enantiomeric carvones. J. Agric. Food Chem., 1971, s. 785–787. DOI: 10.1021/jf60176a035.
- ↑ SRINIVASARAO, Mohan. Chirality and polymers. Current Opinion in Colloid & Interface Science, 1999-04, roč. 4, čís. 2, s. 147–152. Dostupné online [cit. 2022-04-09]. DOI: 10.1016/S1359-0294(99)00024-2. (po anglicky)
- ↑ von Zelewsky, A. (1995). Stereochemistry of Coordination Compounds. Chichester: John Wiley.. ISBN 047195599X.
- ↑ Hartwig, J. F. Organotransition Metal Chemistry, from Bonding to Catalysis; University Science Books: New York, 2010. ISBN 189138953X
- ↑ a b c PUTALA, Martin. NIEKTORÉ ZMENY V NÁZVOSLOVÍ ORGANICKÝCH ZLÚČENÍN [online]. 2008-02-08, [cit. 2022-04-09]. Dostupné online. Archivované 2007-06-23 z originálu.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "enantiomerically enriched (enantioenriched)". DOI:10.1351/goldbook.E02071
- ↑ Eliel, E.L.. Infelicitous Stereochemical Nomenclatures. Chirality, 1997, s. 428–430. Dostupné online [cit. 2016-02-05]. DOI: 10.1002/(sici)1520-636x(1997)9:5/6<428::aid-chir5>3.3.co;2-e. Archivované 2016-03-03 na Wayback Machine
- ↑ a b PUTALA, Martin. NIEKTORÉ ZMENY V NÁZVOSLOVÍ ORGANICKÝCH ZLÚČENÍN [online]. 2008-02-08, [cit. 2022-04-09]. Dostupné online. Archivované 2007-06-23 z originálu.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "asymmetric synthesis". DOI:10.1351/goldbook.E02072
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "enantiomer excess (enantiomeric excess)". DOI:10.1351/goldbook.E02070
- ↑ FRANKEL, Eugene. Corpuscular Optics and the Wave Theory of Light: The Science and Politics of a Revolution in Physics. Social Studies of Science (Sage Publications Inc.), 1976, s. 147–154. Dostupné online.
- ↑ Pasteur, L.. Researches on the molecular asymmetry of natural organic products, English translation of French original, published by Alembic Club Reprints (Vol. 14, pp. 1–46) in 1905, facsimile reproduction by SPIE in a 1990 book. 1848.
- ↑ Eliel, Ernest Ludwig; Wilen, Samuel H.; Mander, Lewis N.. Stereochemistry of Organic Compounds. 1st. vyd. New York, NY, USA : Wiley & Sons, 1994. ISBN 978-0471016700. Chirality in Molecules Devoid of Chiral Centers (Chapter 14).
- ↑ Bentley, Ronald. From Optical Activity in Quartz to Chiral Drugs: Molecular Handedness in Biology and Medicine.. Perspect. Biol. Med., 1995, s. 188–229. DOI: 10.1353/pbm.1995.0069. PMID 7899056.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Optical isomers". DOI:10.1351/goldbook.O04308
- ↑ WERNER, A.. Zur Kenntnis des asymmetrischen Kobaltatoms. I. Berichte der Deutschen Chemischen Gesellschaft, May 1911, s. 1887–1898. Dostupné online. DOI: 10.1002/cber.19110440297. (po nemecky)
- ↑ Odor Incongruity and Chirality. Science, 1971, s. 1044–1046. DOI: 10.1126/science.172.3987.1044. PMID 5573954.
- ↑ Stereochemistry-Odor Relationships in Enantiomeric Ambergris Fragrances. Helvetica Chimica Acta, 1980, s. 1932–1946. DOI: 10.1002/hlca.19800630721.
Literatúra[upraviť | upraviť zdroj]
- Clayden, Jonathan; Greeves, Nick; Warren, Stuart. Organic Chemistry. 2nd. vyd. Oxford, UK : Oxford University Press, 2012. Dostupné online. ISBN 978-0199270293. S. 319f, 432, 604np, 653, 746int, 803ketals, 839, 846f.
- Eliel, Ernest Ludwig; Wilen, Samuel H.; Mander, Lewis N.. Stereochemistry of Organic Compounds. 1st. vyd. New York, NY, USA : Wiley & Sons, 1994. ISBN 978-0471016700. DOI:<428::AID-CHIR5>3.0.CO;2-1 10.1002/(SICI)1520-636X(1997)9:5/6<428::AID-CHIR5>3.0.CO;2-1 Chirality in Molecules Devoid of Chiral Centers (Chapter 14), s. 428–430.
- Eliel, E.L.. Infelicitous Stereochemical Nomenclatures. Chirality, 1997, s. 428–430. Dostupné online [cit. 2016-02-05]. DOI: 10.1002/(SICI)1520-636X(1997)9:5/6<428::AID-CHIR5>3.0.CO;2-1. Archivované 2016-03-03 na Wayback Machine
- Gal, Joseph. Differentiation of Enantiomers I. [s.l.] : [s.n.], 2013. ISBN 978-3-319-03238-2. DOI:10.1007/128_2013_435 Molecular Chirality: Language, History, and Significance, s. 1–20.
Zdroj[upraviť | upraviť zdroj]
Tento článok je čiastočný alebo úplný preklad článku Chirality (chemistry) na anglickej Wikipédii.