Cis-trans izoméria


Cis–trans izoméria je výraz používaný v organickej chémii. Predpony „cis“ a „trans“ pochádzajú z latinčiny a znamenajú „na tejto strane“ a „na opačnej strane“.[1] V chémii sa využíva predpona cis pre označenie funkčných skupín (substituentov) na rovnakej strane roviny, zatiaľ čo predpona trans označuje funkčné skupiny na opačných stranách. Cis-trans izoméry sú stereoizoméry, teda páry molekúl, ktoré majú rovnaký vzorec, ale rôzne rozloženie funkčných skupín v trojdimenzionálnom priestore. Označenie cis-trans nemusí vždy odpovedať E-Z izomérii, ktorá je absolútnym stereochemickým popisom. Všobecne sa označenie cis/trans používa u stereomérov, ktoré obsahujú dvojitú väzbu, okolo ktorej nie je možná rotácia, alebo cyklickú štruktúru, kde je obmedzená alebo nemožná rotácia jednotlivých väzieb.[2] Cis a trans izoméry sa vyskytujú v organických molekulách i anorganických koordinačných komplexoch. Deskriptory cis a trans sa nepoužívajú v prípade konformačných izomérov, kde sa môžu jednotlivé geometrické formy jednoducho premieňať jedna na druhú, ako sú lineárne molekuly s jednoduchými väzbami. U podobných štruktúr sa namiesto toho používajú deskriptory „syn“ a „anti“.
Použitie v organickej chémii[upraviť | upraviť zdroj]
Ak sú substituenty orientované rovnakým smerom, daný diastereomér je označovaný ako cis, zatiaľ čo v prípade substituentov orientovaných opačnými smermi sa využíva označenie trans. Príkladom takého uhľovodíku je napríklad but-2-én. Metylové skupiny viazané na uhlíky spojené dvojitou väzbou môžu byť oba na jednej strane (cis), alebo každý na opačnej strane (trans).
Cis-trans izoméria môže byť prítomná i v alicyklických zlúčeninách. Príkladom takej štruktúry môže byť napríklad 1,2-dichlorocyklohexán:
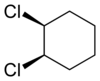 
|
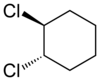 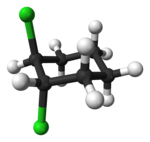
|
| cis-1,2-dichlorocyklohexán | trans-1,2-dichlorocyklohexán |
Porovnanie fyzikálnych vlastností[upraviť | upraviť zdroj]
Cis a trans izoméry majú často odlišné vlastnosti. Všeobecne je rozdiel vo vlastnostiach spôsobený rôznymi tvarmi molekúl alebo napríklad zmenou celkového dipólového momentu.

|

|
| cis-2-pentén | trans-2-pentén |
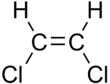
|

|
| cis-1,2-dichloroetén | trans-1,2-dichloroetén |

|
|
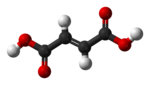
| kyselina cis-buténdiová (kyselina maleínová) |
kyselina trans-butándiová (kyselina fumarová) |
|

|
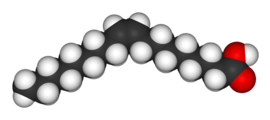
| Kyselina oleínová | Kyselina elaidová |
Niektoré rozdiely môžu byť nevýrazné, ako je to napríklad pri bode varu krátkych alkénov, ako je pent-2-én. Bod varu cis izoméru je 37°C, zatiaľ čo u trans izoméru je to 36 °C.[3] Rozdiel môže byť väčší u izomérov, ktoré majú polárne väzby, ako je 1,2-dichloretén. Bod varu cis izoméru je 60,3 °C, ale u trans izoméru je to len 47,5 °C.[4] V prípade cis zoméru dochádza k sčítaniu dipólových momentov C-Cl väzieb, na základe čoho má molekula celkový dipól. Vďaka nemu existujú medzimolekulárne dipól-dipólové interakcie (Keesomove sily), ktoré sa skladajú s Londonovými dispeznými silami a zvyšujú bod varu. U trans izoméru sú však dipólové momenty C-Cl väzieb orientované opačným smerom, takže dochádza ich k odčítaniu a molekula teda nemá žiadny výsledný dipólový moment (má však nenulový kvadrupólový moment).
V prípade kyseliny buténdiovej sú rozdiely vo vlastnostiach a reaktivite izomérov tak veľké, že jednotlivé izoméry dostali rôzne názvy. Cis izomér sa označuje ako kyselina maleínová, zatiaľ čo trans izomér je známy ako kyselina fumarová. Kľúčovou vlastnosťou v určovaní relatívneho bodu varu je polarita, ktorá zvyšuje medzimolekulárne sily, čím sa zvyčuje bod varu. Podobným spôsobom ovplvyvňuje symetria štruktúry bod topenia, keďže vďaka nej sa môžu molekuly lepšie poskladať v pevnom stave, aj keď symetria nemení polaritu molekuly. Takým prípadom je napríklad kyseliny oleínová a elaidová. Kyselina oleínová je cis izomér, ktorá má bod topenia 13,4 °C, čo znamená, že je pri izbovej teplote tekutá. Kyselina elaidová je trans izomér a jej bod topenia je 43 °C, keďže rovný tvar molekuly umožňuje lepšie skladanie molekúl k sebe, na základe čoho je pri izbovej teplote tuhá.
Mnohé iné trendy je možné vypozorovať u cis-trans izomérov, hlavne ako dôsledky dvojitých väzieb a substituentov ležiacich na jej rôznych stranách, predovšetkým ak sú substituenty rovnaké. Tieto trendy vznikajú hlavne ako dôsledok toho, že u cis izomérov dochádza k skladaniu dipólových momentov, zatiaľ čo u trans izomérov sa dipólový moment vyruší.[5] Trans alkény, ktoré sú menej polárne a zvyčajne viac symetrické, teda majú nižšie body varu a vyššie teploty topenia. Naproti tomu cis alkény, ktoré sú zvyčajne polárnejšie a menej symetrické, majú naopak vyššie body varu a nižšie teploty topenia. Všeobecne majú trans alkény vyššie body topenia a nižšiu rozpustnosť v inertných rozpúšťadlách, keďže sú symetrickejšie oproti cis alkénom.[6] Podobne zvyknú mať trans izoméry nižšiu hustotu v porovnaní s cis izomérmi.[chýba zdroj]
Stabilita[upraviť | upraviť zdroj]
Trans izoméry sú pre acyklické zlúčeniny zvyčajne stabilnejšie, než cis izoméry. Toto je spôsobené hlavne nevhodnými stérickými interakciami substituentov cis izoméru. Kvôli tomu majú trans izoméry menej exotermické spaľné teplo, čo naznačuje vyššiu termochemickú stabilitu.[6] Niekedy môže byť cis izomér stabilnejší ako trans izomér, čo sa označuje ako cis efekt.[7] Príkladom takých zlúčenín je napríklad 1,2-difluoroetylén alebo 1,2-difluorodiazén (FN=NF) a niektoré ďalšie halogénmi alebo kyslíkom substituiované etylény.
E/Z zápis[upraviť | upraviť zdroj]
Cis-trans názvoslovie by sa malo využívať len pre alkény, u ktorých je jednoznačné, ktoré substituenty sú popisované navzájom voči sebe. U zložitejších prípadov sa pomenovanie cis/trans zvyčajne určuje podľa najdlhšieho uhlíkového reťazca, ktorý zároveň vystupuje v názve zlúčeniny. Naproti tomu je E-Z pomenovanie, ktoré je štandardom IUPAC, vždy jednoznačné, hlavne v prípadoch tri- či tetrasubstituovaných alkénov. Jeho použitím je tak možné predísť akýmkoľvek problémom s určovaním relatívnej polohy substituentov.

Z (z nemeckého zusammen) znamná „spolu“, E (z nemeckého entgegen) znamná „naproti“. Ak sú skupiny s vyššiou prioritou voči sebe cis (teda orientované na tú istú stranu), jedná sa o Z, a ak sú skupiny s vyššiou prioritou voči sebe trans (orientované na opačné strany), jedná sa o E. Konfigurácie E/Z je určená pravidlami CIP - vyššie atómové číslo má vyššiu prioritu. Pre každý z dvoch atómov v dvojitej väzbu je nutné určiť prioritu každého substituentu. Ak sú oba substituenty s vyššiou prioritou na tej istej strane, jedná sa o Z usporiadanie; ak sú na opačnej strane, jedná sa o E.
Keďže pri cis/trans a E-Z názvosloviach sa porovnávajú rôzne skupiny, nemusia si navzájom odpovedať. Neplatí teda, že cis izomér je vždy Z a trans izomér je vždy E. V prípade trans-2-chlorobut-2-énu (dve metylové skupiny, C1 a C4, viazané na but-2-énovú kostru, sú navzájom trans) je (Z)-2-chlorobut-2-én (pretože chlór a C4 sú na rovnakej strane, keďže C1 a C4 sú na opačných stranách).
Použitie v anorganickej chémii[upraviť | upraviť zdroj]
Cis-trans izoméria sa môže vyskytnúť i v anorganických zlúčeniných, typicky v azozlúčeninách a koordinačných komplexoch.
Azozlúčeniny[upraviť | upraviť zdroj]
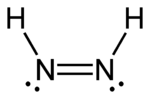
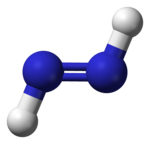
Azozlúčeniny (tiež nazývané diazény, podľa diazénu; a ich príbuzné difosfény) takisto vykazujú túto izomériu. Podobne ako u organických zlúčenín je cis izomér ten reaktívnejší, ktorý ako jediný môže redukovať alkény a alkíny na alkány, ale z iného dôvodu: trans izomér nemôže vhodne orientovať svoje vodíky tak, aby mohol redukovať alkén, zatiaľ čo cis izomér môže, keďže má iný tvar.
|
|
| cis-diazén | trans-diazén |
Koordinačné komplexy[upraviť | upraviť zdroj]
V anorganických koordinačných komplexoch s oktahedrálnou alebo štvorcovo planárnou geometriou takisto existujú cis izoméry, ktoré majú podobné ligandy blízko u seba, a trans izoméry, ktoré majú podobné ligandy ďalej od seba.
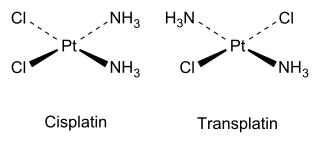
Príkladom sú napríklad štvorcovo planárne izoméry Pt(NH3)2Cl2, popísané Alfredom Wernerom v roku 1893. Barnett Rosenberg v roku 1969 ukázal antitumorovú aktivitu cis izoméru, ktorého celý názov je cis-diamíndichloroplatinitan, na základe čoho je tento izomér používaný ako liek pri chemoterapii pod názvom cisplatina. Naproti tomu trans izomér nemá významnú aktivitu proti rakovine. S využitím trans efektu je pri syntéze možné dosiahnuť požadovaný izomér.
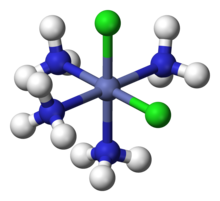
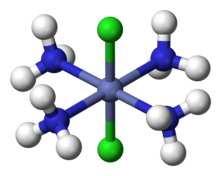
U oktahedrálnych komplexov so vzorcom MX4Y2 (kde M je atóm kovu a X a Y sú dva rôzne druhy ligandov) existujú dva izoméry. V prípade cis izoméru zvierajú Y ligandy uhol 90°, zatiaľ čo v trans izomére zvierajú tieto ligandy uhol 180°. Príkladom takéhoto komplexu je napríklad cis-[Co(NH3)4Cl2]+.
|
|
| cis-[Co(NH3)4Cl2]+ | trans-[Co(NH3)4Cl2]+ |
Podobným typom izomérie je faciálne-meridionálna (fac/mer) izoméria v komplexoch so všeobecným vzorcom MX3Y3, u ktorých je iný počet ligandov orientovaný cis/trans voči sebe. Karbonylové zlúčeniny kovov je možné charakterizovať ako „fac“ alebo „mer“ pomocou infračervenej spektroskopie.
Referencie[upraviť | upraviť zdroj]
- ↑ Charlton T. Lewis, Charles Short, A Latin Dictionary (Clarendon Press, 1879) Entry for cis
- ↑ REUSCH, William. Stereoisomers Part I [online]. Michigan State University, 2010. Dostupné online.
- ↑ Chemicalland values [online]. Chemicalland21.com. Dostupné online.
- ↑ CRC Handbook of Chemistry and Physics. 60th. vyd. [s.l.] : [s.n.], 1979–1980. S. C-298.
- ↑ OUELLETTE, Robert J.; RAWN, J. David. Principles of Organic Chemistry. [s.l.] : [s.n.], 2015. ISBN 978-0-12-802444-7. DOI:10.1016/B978-0-12-802444-7.00004-5 Alkenes and Alkynes, s. 95–132.
- ↑ a b MARCH, Jerry. Advanced Organic Chemistry, Reactions, Mechanisms and structure. 3rd. vyd. [s.l.] : [s.n.], 1985. ISBN 978-0-471-85472-2. S. 111.
- ↑ Contribution to the Study of the Gauche Effect. The Complete Structure of the Anti Rotamer of 1,2-Difluoroethane. J. Am. Chem. Soc., 1997, s. 4789. DOI: 10.1021/ja963819e.
Pozri aj[upraviť | upraviť zdroj]
Externé odkazy[upraviť | upraviť zdroj]
- IUPAC definícia „stereoisomerism“
- IUPAC definícia „geometric isomerism“
- IUPAC definícia „cis–trans isomers“
Zdroj[upraviť | upraviť zdroj]
Tento článok je čiastočný alebo úplný preklad článku Cis–trans isomerism na anglickej Wikipédii.
