Sulfónamid (chémia)
- Nezamieňať s heslom sulfamid.

Sulfónamid[1][2][3] je funkčná skupina, ktorá pozostáva zo sulfonylovej skupiny viazanej na amínovú skupinu, teda RS(=O)2-NH2. Táto skupina je relatívne nereaktívna a jej amínová skupina nie je zásaditá. Väzba S-N sa štiepi ťažko a kvôli pevnosti tejto skupiny sú sulfónamidy zvyčajne kryštalické. Kvôli tomu je tvorba sulfónamidu jednou z klasických metód premeny amínu na kryštalický derivát, ktorý sa dá identifikovať podľa bodu topenia. Mnoho dôležitých liekov obsahuje sulfónamidovú skupinu.[4]
Sulfónamidy ako zlúčeniny obsahujú sulfónamidovú skupinu. Ich všeobecný vzorec je RSO2NR2, kde R je nejaká organická skupina. Príkladom je metánsulfónamid, ktorého vzorec je CH3SO2NH2. Sulfónamidy sa všeobecne dajú považovať za deriváty sulfónových kyselín, u ktorých bola hydroxylová skupina nahradený za amínovú skupinu. Prvý sulfónamid bol syntetizovaný v Nemecku v roku 1932.[5]
Syntéza[upraviť | upraviť zdroj]
Sulfónamidy je možné pripraviť v laboratóriu mnohými spôsobmi. Bežným postupom prípravy je reakcia sulfonylchloridu s amínom:
- RSO2Cl + R2NH → RSO2NR2 + HCl
Zvyčajne sa do roztoku pridáva zásada, napríklad pyridín, ktorá neutralizuje kyselinu chlorovodíkovú, ktorá vzniká v procese. Jedným z príkladov tejto syntézy je príprava sulfonylmetylamidu.[6] Tozylchlorid sa používa ako bežný zdroj sulfonylchloridu.[7] Reakcia primárnych a sekundárnych amínov s benzénsulfonylchloridom je základom Hinsbergovej reakcie, ktorá umožňuje detekciu primárnych a sekundárnych amínov.
Sultámy[upraviť | upraviť zdroj]
Sultámy sú cyklické sulfónamidy. Sú obdobou laktónov (cyklických esterov karboxylových kyselín) a laktámov (cyklických karboxamidov). Medzi bioaktívne sultámy patria ampiroxikam, ktorý pôsobí proti zápalom, a sulthiam, antikonvulzant. Sultámy sa pripravujú analogicky k ostatným sulfónamidom, keďže amíny deprotonujú sulfónové kyseliny. Často sa pripravujú oxidáciou disulfidov alebo tiolov viazaných na amíny v jednej reakčnej nádobe.[8] Alternatívnym spôsobom syntézy sultámov je počiatočná príprava lineárneho sulfónamidu a následná intramolekulárna reakcia, pri ktorej vzniká C-C väzby (teda cyklizácia). Tento spôsob syntézy bol využitý pre tvorbu tmavomodrého emiteru pre organickú elektroniku založeného na sultámoch.[9]
- Zlúčeniny so sulfónamidovou funkčnou skupinou
-
Sacharín, cyklický sulfónamid, jedno z prvých objavených umelých sladidiel.
-
Sulfanilamid, zlúčenina, ktorá inšpirovala vývoj mnohých liečiv.
-
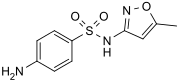
Sulfametoxazol, antibiotikum.
-
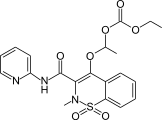
Ampiroxikam, sultám používaný ako liek proti zápalom.
-
Hydrochlorotiazid, liečivo obsahujúce acyklickú i cyklickú sulfónamidovú skupinu.
-
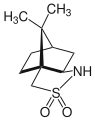
Kamforsultám, sultám používaný pri chirálnej organickej syntéze.
Disulfónimidy[upraviť | upraviť zdroj]
Disulfónimidy majú vzorec R-S(=O)2-N(H)-S(=O)2-R' a majú dve sulfónové skupiny napojené na ten istý amín.[10] Podobne ako u sulfónamidov i tieto zlúčeniny sa používajú ako činidlá pri enantioselektívnej syntéze.[10][11][12]
Bis(trifluórometánsulfonyl)anilín je zdroj triflylovej skupiny (CF3SO2+).
Sulfínamidy[upraviť | upraviť zdroj]
Sulfínamidy, R(S=O)NHR, sú amidy sulfínových kyselín, R(S=O)OH. Chirálne sulfínamidy, napríklad terc-butánsulfínamid, p-toluénsulfínamid[13][14] a 2,4,6-trimetylbenzénsulfínamid[15] sú činidlá používané pri asymetrickej syntéze.
Referencie[upraviť | upraviť zdroj]
- ↑ sulfónamid | slovensky.eu [online]. Slovensky, 2018-01-01, [cit. 2022-03-08]. Dostupné online.
- ↑ GARAJ, Vladimír. Molekulové kotvenie virtuálnej kombinatorickej knižnice nových sulfónamidov do aktívneho miesta karboanhydrázy Mycobacterium tuberculosis [online]. arl4.library.sk, [cit. 2022-03-08]. Dostupné online.
- ↑ MIKLÁŠ, Roman. Syntéza a štúdium antimikróbnej aktivity amfifilných imidazóliových sulfónamidov odvodených od kyseliny (+)-gáfor-10-sulfónovej [online]. arl4.library.sk, [cit. 2022-03-08]. Dostupné online.
- ↑ ACTOR, Paul; CHOW, Alfred W.; DUTKO, Frank J.. Chemotherapeutics. Weinheim, Germany : Wiley-VCH Verlag GmbH & Co. KGaA, 2000-06-15. Dostupné online. DOI:10.1002/14356007.a06_173
- ↑ LEVY, Stuart B.. The antibiotic paradox : how the misuse of antibiotics destroys their curative powers. 2. vyd. Cambridge, Massachusetts : Perseus Publ., 2002. Dostupné online. ISBN 9780738204406. S. 51. [nefunkčný odkaz]
- ↑ Organic Syntheses, Coll. Vol. 4, p.943 (1963); Vol. 34, p.96 (1954). Online Article
- ↑ Organic Syntheses, Coll. Vol. 5, p.39 (1973); Vol. 48, p.8 (1968) Online Article
- ↑ RASSADIN, V. A.; GROSHEVA, D. S.; TOMASHEVSKII, A. A.. Methods of Sultam Synthesis. Chemistry of Heterocyclic Compounds, 2013-04, roč. 49, čís. 1, s. 39–65. Dostupné online [cit. 2022-03-08]. ISSN 0009-3122. DOI: 10.1007/s10593-013-1231-3. (po anglicky)
- ↑ Sultam-Based Hetero[5]helicene: Synthesis, Structure, and Crystallization-Induced Emission Enhancement. ACS Omega, 2016, s. 1336–1342. DOI: 10.1021/acsomega.6b00335. PMID 31457199.
- ↑ a b Development and Applications of Disulfonimides in Enantioselective Organocatalysis. Chem. Rev., 2015, s. 9388–9409. DOI: 10.1021/acs.chemrev.5b00128.
- ↑ BINBAM – A New Motif for Strong and Chiral Brønsted Acids. Eur. J. Org. Chem., 2009, s. 3693–3697. DOI: 10.1002/ejoc.200900548.
- ↑ A Powerful Chiral Counteranion Motif for Asymmetric Catalysis. Angew. Chem. Int. Ed., 2009, s. 4363–4366. DOI: 10.1002/anie.200901768.
- ↑ Organic Syntheses, Coll. Vol. 10, p.47 (2004); Vol. 77, p.50 (2000). Link
- ↑ Org. Synth. 2007, 84, 129-138 Link
- ↑ Org. Synth. 2006, 83, 131-140 Link
Pozdi aj[upraviť | upraviť zdroj]
Zdroj[upraviť | upraviť zdroj]
Tento článok je čiastočný alebo úplný preklad článku Sulfonamide na anglickej Wikipédii.