Ribozóm
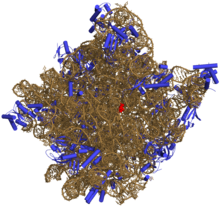

1. Jadierko
2. Jadro
3. Ribozóm (malé bodky)
4. Vezikula
5. Drsné endoplazmatické retikulum
6. Golgiho aparát
7. Cytoskelet
8. Hladké endoplazmatické retikulum
9. Mitochondria
10. Vakuola
11. Cytosól (spolu s ostatnými organelami tvorí cytoplazmu)
12. Lyzozóm
13. Centrozóm spolu s centriolami
14. Cytoplazmatická membrána
Ribozómy sú bunkové organely nachádzajúce sa vo všetkých známych bunkách, čiže vo všetkých živých organizmoch okrem vírusov, pokiaľ sú pokladané za živé. Prebieha v nich syntéza bielkovín (proteínov) – proteosyntéza. Patria medzi najhojnejšie zastúpené bunkové organely. Sú uložené voľne v cytoplazme, u eukaryotov sú tiež vnútri plastidov, mitochondrií a viazané na endoplazmatické retikulum. Obsahujú ribonukleovú kyselinu (RNA) a bielkoviny, z chemického hľadiska preto patria medzi nukleoproteíny.
Bielkoviny tvoria cca 1/3 obsahu ribozómu. Odlišujeme dva základné typy týchto organel (pre prokaryoty a eukaryoty). Eukaryoty však majú v semiautonómnych organelách ribozómy podobné prokaryotickým ribozómom a iba ich cytoplazmatické ribozómy sa označujú ako ribozómy eukaryotického typu. Každý ribozóm sa delí na dve podjednotky s odlišnými veľkosťami. K ribozómu sa napája tzv. mediátorová ribonukleová kyselina (mRNA), ktorá obsahuje prepis genetickej informácie z deoxyribonukleovej kyseliny (DNA). Ribozóm potom podľa tejto informácie nasyntetizuje polypeptid resp. proteín. Proces jeho syntézy sa nazýva translácia a prebieha tak, že ribozóm sa pohybuje pozdĺž mRNA a prekladá jej kodóny do peptidového reťazca. Po pripojení každej aminokyseliny k peptidovému reťazcu dochádza k posunu ribozómu po mRNA o tri nukleotidy (kodón) smerom k 3´ koncu, čo sa označuje ako translokácia ribozómu.[1] V prokaryotických bunkách sa ribozóm pohybuje po mRNA rýchlosťou 30 – 60 nukleotidov za sekundu, v eukaryotických je to len 9 až 15 nukleotidov/sek.[2]
Počet ribozómov v bunkách je veľmi variabilný. V baktérii Escherichia coli ich napríklad je priemerne asi 15 000.[3] Jedna molekula mRNA môže byť súčasne translatovaná viacerými ribozómami. V prípade, že je na jednu mRNA nadviazaných viac ribozómov, hovoríme o polyribozóme alebo o polyzóme.
Objav
[upraviť | upraviť zdroj]Ribozómy boli prvýkrát pozorované v polovici 50. rokov rumunsko-americkým cytológom Georgom Emilom Paladim pomocou elektrónového mikroskopu ako husté častice alebo granuly.[4] Termín „ribozóm“ navrhol vedec Richard B. Roberts koncom 50. rokov 20. storočia:
„V priebehu sympózia sa objavili sémantické problémy. Pre niektorých účastníkov „mikrozómy“ znamenajú častice ribonukleoproteínu mikrozómovej frakcie kontaminované inými proteínmi a lipidmi, pre ostatných mikrozómy pozostávajú z proteínov a lipidov kontaminovaných časticami. Fráza „mikrozomálne častice“ sa nezdá byť primeraná a „ribonukleoproteínové častice z frakcie mikrozómov“ je značne zvláštna. Počas stretnutia bolo navrhnuté slovo „ribozóm“, ktoré je vyhovujúce a taktiež príjemne znejúce. Súčasné zmätenie by bolo eliminované, ak by sa prijal „ribozóm“ na označenie ribonukleoproteínových častíc vo veľkosti od 35 do 100 S.“
- Albert, Mikrosomálne častice a syntéza proteínov[5]
Albert Claude, Christian de Duve a George Emil Palade získali spoločne Nobelovu cenu za fyziológiu alebo medicínu v roku 1974 za objav ribozómu.[6] Nobelova cena za chémiu v roku 2009 bola udelená Venkatramanovi Ramakrishnanovi, Thomasovi A. Steitzovi a Ade E. Jonathovej za stanovenie podrobnej štruktúry a funkcie ribozómu.[7]
Vznik
[upraviť | upraviť zdroj]Ribozómy sú zložené z ribozomálnych proteínov a z ribozomálnej RNA (rRNA). Ribozomálne proteíny sa syntetizujú na už existujúcich ribozómoch v cytoplazme bunky. Po ich vytvorení sú tieto proteíny v eukaryotických bunkách dopravené do jadra bunky. Tam sa spájajú s novosyntetizovanou rRNA už pred dokončením jej vzniku transkripciou. Takto sa skopmletizujú celé podjednotky ribozómov a následne sú dopravené opäť do cytoplazmy, kde sa zúčastňujú proteosyntézy.[8]
Gény pre rRNA sú najaktívnejšie prepisované vtedy, keď (bakteriálna) bunka podstupuje rýchle delenie, ktoré je prirodzene spojené s veľkou potrebou proteínov. V rýchlo rastúcich bakteriálnych kultúrach môžu tvoriť ribozómy aj viac ako tretinu ich hmoty. Transkripciu rRNA u baktérií reguluje guanozín-5´-bisfosfát-3´bisfosfát, skrátene ppGpp. Pri nedostatku ppGpp intenzívne prebieha syntéza rRNA, ale pri jeho nadbytku sa zastaví. ppGpp pravdepodobne pôsobí na RNA-polymerázu, ktorá v jeho prítomnosti stráca afinitu k promótoru génu pre rRNA.[1]
Stavba ribozómu
[upraviť | upraviť zdroj]Ribozóm je malá bunková organela s priemerom 17 až 20 nm, preto je pozorovateľný len elektrónovým mikroskopom. Možno ich z bunky separovať mechanickým rozdrvením bunky skleným práškom alebo enzymatickým rozrušením bunkovej steny. V rastlinných a živočíšnych bunkách sú všetky ribozómy prisadnuté na membránach.[9]
Ribozóm sa približne z dvoch tretín skladá z ribonukleovej kyseliny (konkrétne tzv. rRNA, teda ribozomálnej RNA), a zvyšnú tretinu tvoria proteíny.[10] Všetky organizmy majú podobnú stavbu ribozómov.[11] Bielkoviny a molekuly rRNA sú navzájom spojené iónovými väzbami a vodíkovými väzbami.[2] U prokaryotov sa ribozómy skladajú z 65 % rRNA a 35 % proteínov, ribozómy endoplazmatického retikula eukaryotov obsahujú 55 % rRNA a 45 % proteínov.[3]

Všetky ribozómy možno rozdeliť na dve základné časti, na malú a veľkú podjednotku (subjednotku). Napriek tomu však existujú určité rozdiely, hlavne v stavbe, medzi prokaryotickými a eukaryotickými ribozómami. Pod pojmom eukaryotický ribozóm sa myslia ribozómy umiestnené mimo plastidov a mitochondrií. Ribozómy plastidov a mitochondrií sa totiž podobajú prokaryotickým ribozómom, z ktorých pravdepodobne vznikli, svojou sedimentačnou konštantou aj spôsobom translácie.
Rozdiely medzi ribozómami sa veľmi často udávajú pomocou tzv. sedimentačného koeficientu, čiže veličiny, ktorá udáva čas, za ktorý v ultracentrifúge prebehne sedimentácia ribozómu. Jednotkou je Svedberg (S), a táto jednotka predstavuje čas 10−13 sekundy. Prokaryotický ribozóm sa na základe týchto veličín označuje ako 70S, eukaryotický je 80S.[11] Tiež obe podjednotky vykazujú určité rozdiely, pokiaľ porovnáme sedimentačné koeficienty eukaryotických a prokaryotických ribozómov. Taktiež ribozomálna RNA sa rozlišuje na základe sedimentácie; u prokaryotov poznáme 5S, 16S a 23S rRNA.[1]
Podjednotky sú spolu a utvárajú ribozóm len počas proteosyntézy. Po jej skončení sa rozpadajú na samostatné podjednotky, ktoré sú zrejme až do ďalšieho spojenia s mRNA v bunke vo voľnom stave.[12][13] Na podjednotky ribozómy disociujú napríklad za zníženej koncentrácie iónov draslíka.[3] Spojeniu oboch jednotiek u prokaryotov bráni iniciačný faktor IF3, ktorý sa naviaže na malú podjednotku. Tento faktor ale zároveň umožňuje, aby sa naň nadviazal komplex zložený z iniciačného faktoru IF2, guanozíntrifosfátu (GTP) a tRNA nesúcej formylovaný metionín.[1] Malá podjednotka je teda pripravená zahájiť iniciáciu translácie.
Malá podjednotka
[upraviť | upraviť zdroj]Úlohou malej podjednotky je nasadiť tRNA na kodóny mRNA v procese translácie.[8] Malá podjednotka prokaryotov má koeficient 30S, u eukaryotov je táto podjednotka 40S. Za začiatok translácie peptidového reťazca sa považuje okamih, keď sa táto malá podjednotka naviaže na mRNA. To sa deje skôr ako nadviazanie veľkej podjednotky. Pripojenie veľkej podjednotky je umožnené len po nadviazaní mRNA a prvej (iniciačnej) molekuly transferovej ribonukleovej kyseliny (tRNA). Tieto udalosti spôsobia zmenu konformácie malej podjednotky. Malá podjednotka v priebehu translácie sprostredkováva dekódujúcu interakciu medzi kodónom na mRNA a antikodónom na tRNA.[2]
Veľká podjednotka
[upraviť | upraviť zdroj]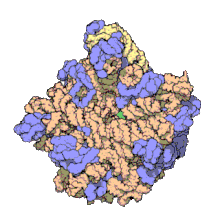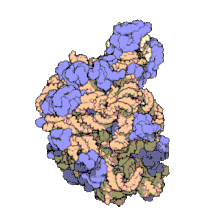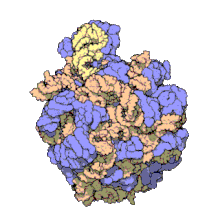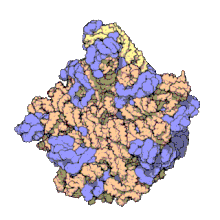
Veľká podjednotka slúži počas translácie na katalyzovanie vzniku peptidovej väzby medzi aminokyselinou a vznikajúcim reťazcom.[8] Veľká podjednotka ribozómu je u prokaryotov 50S, u eukaryotov 60S.[11] Veľká podjednotka sa pripája na tzv. prediniciačný komplex zložený z iniciačných faktorov, RNA a malej podjednotky. Spojením veľkej a malej podjednotky sa ribozóm kompletizuje a vzniká tzv. iniciačný komplex, ktorý prechádza v translácii do fázy elongácie. Podjednotky sa spájajú v blízkosti 5´ konca mRNA.[8] Vo veľkej podjednotke je akýsi „tunel“, v ktorom zostáva skrytý rastúci peptidový reťazec, až kým nedosiahne dĺžku približne 70 aminokyselín. Až vtedy sa jeho N-koniec vynára von z ribozómu.
Väzobné miesta
[upraviť | upraviť zdroj]V ribozóme sa nachádzajú celkove 4 väzobné miesta pre molekuly RNA: jedno pre mRNA a tri pre aktivované formy tRNA (aminoacyl-tRNA, skrátene aa-tRNA). Väzobné miesto pre mRNA sa nachádza na malej podjednotke,[1] komplexy aminoacyl-tRNA sa z veľkej časti viažu na styčnom mieste oboch podjednotiek. Táto styčná plocha je bohatšia na rRNA a chudobnejšia na ribozómové bielkoviny ako ostatné časti ribozómu.[2] Miesta pre tRNA sú označené ako aminoacylové (A), peptidylové (P) a výstupné (E) miesto.[1][8] Aminoacylové miesto sa nachádza z menšej časti na malej podjednotke, z väčšej časti na väčšej podjednotke a vstupujú doň aa-tRNA. Odtiaľ sa presunú na pepitdylové miesto, ktoré je, podobne ako A miesto, lokalizované z menšej časti na menšej podjednotke a z väčšej časti na väčšej podjednotke. Na toto miesto sa viaže tRNA, ktorej aminokyselina je už spojená so vznikajúcim peptidovým reťazcom, ale stále pretrváva aj esterová väzba medzi 3´ tRNA, ktorá najnovšiu aminokyselinu doniesla. Po oddelení sa tRNA od aminokyseliny tRNA postupuje na E miesto, ktorého názov je odvodený z anglického slova exit (východ), pretože cezeň deacetylovaná tRNA opúšťa ribozóm. Vznik peptidovej väzby medzi prichádzajúcimi aminokyselinami sa uskutočňuje na peptidyltransferázovom mieste.[1]
Ďalej sa na ribozóme nachádzajú väzobné miesta pre ďalšie nevyhnutné súčasti translácie – iniciačné a elongačné faktory.[1] Vnútorná hmota ribozómu sa označuje ako dreň (core).
rRNA
[upraviť | upraviť zdroj]Ribozomálna RNA je esenciálnou zložkou ribozómov. Zistilo sa, že práve rRNA je zodpovedná za funkčnosť ribozómu, čiže jeho schopnosť prepisovať mRNA do proteínov. Z tohto pohľadu je ribozomálna RNA vlastne enzým a preto sa nazýva ribozým. Objav tejto funkcie bol spočiatku prekvapivý, pretože sa myslelo, že enzymatickej aktivity sú schopné len proteíny. Ribozomálna RNA však tvorí priestorové štruktúry, podobné aktívnym miestam proteínov fungujúcich ako enzýmy. Vďaka tomu je schopná napríklad správne nadviazať aa-tRNA a taktiež zaisťuje vznik peptidových väzieb medzi aminokyselinami vznikajúceho reťazca (druhú z menovaných ovláda u prokaryotov predovšetkým 23S rRNA).

Prokaryotický a eukaryotický ribozóm sa však v obsahu rRNA líšia. Zatiaľ čo prokaryotický obsahuje v malej podjednotke 16S rRNA (1540 nukleotidov) a vo veľkej podjednotke 5S rRNA (120 nukleotidov) a 23S rRNA (2900 nukleotidov), eukaryotický obsahuje v malej podjednotke 18S rRNA (1 900 nukleotidov) a vo veľkej podjednotke 5S rRNA (120 nukleotidov), 5,8S rRNA (160 nukleotidov) a 28S rRNA (4 700 nukleotidov).[11] 16S rRNA je zložkou A miesta ribozómu.[1]
Proteíny
[upraviť | upraviť zdroj]Ribozómy sa skladajú tiež z proteínov. Prokaryotické ribozómy obsahujú 55 proteínov (21 v malej a 34 vo veľkej podjednotke), eukaryotické majú dokonca 82 proteínov (33 v malej a 49 vo veľkej podjednotke).[11] Bielkoviny ribozómov majú prevažne kladný náboj, ale nie sú blízke histónom. Obsahujú veľký počet lyzínových a arginínových zvyškov.[3] Mnohé z nich majú dosť neobvyklú štruktúru s dlhými roztiahnutými ramenami obohatenými o bázické bielkoviny. Tie pravdepodobne umožňujú zvinutie negatívne nabitej fosfátovej kostry rRNA do kompaktnej priestorovej štruktúry.
Ribozomálne proteíny možno rozdeliť na
- jednotkové – vyskytujú sa v každom ribozóme v jednej až dvoch kópiách. Majú hlavne štruktúrnu funkciu – tvoria kostru obidvoch podjednotiek.[3]
- okrajové – nevyskytujú sa v každom ribozóme, frekvencia ich výskytu je 0,5 až 0,8 molekuly na jeden ribozóm
- zlomkové – frekvencia ich výskytu je menšia ako 0,5
Niektoré ribozomálne proteíny sú asociované so špecifickými väzobnými miestami:
- A miesto – jeho súčasťou sú proteíny L1, L5, L7, L12, L30, L33
- P miesto – jeho súčasťou sú proteíny L7, L12, L14, L18, L24, L33[1]
Bakteriálne ribozómy
[upraviť | upraviť zdroj]Prokaryotické ribozómy majú priemer približne 20 nm.[14] Kryštalografickou analýzou[15] bolo preukázané, že v blízkosti reakčného miesta pre syntézu polypeptidov nie sú žiadne ribozomálne proteíny. To naznačuje, že proteínové zložky ribozómov sa priamo nepodieľajú na katalýze tvorby peptidových väzieb, ale že tieto proteíny pôsobia ako lešenie, ktoré môže zosilniť schopnosť rRNA podieľať sa na syntéze proteínov.
Technikou afinitného značenia ribozomálnych proteínov E. coli bolo zistené, že proteíny L27, L14, L15, L16, L2 sú lokalizované vo väzobnom mieste alebo v blízkosti väzobného miesta pre tRNA (A a P miesta) vo veľkej podjednotke ribozómu.[16][17]
Proteíny S1 a S21, v spojení s 3'-koncom 16S rRNA, sú zapojené do iniciácie (začiatku) translácie.[18]
| Ribozóm | Podjednotka | Molekuly rRNA | Ribozomálne proteíny |
|---|---|---|---|
| 70S | 50S | 23S (2904 nukleotidov) | 31 |
| 5S (120 nukleotidov) | |||
| 30S | 16S (1542 nukleotidov) | 21 |
Eukaryotické ribozómy
[upraviť | upraviť zdroj]Eukaryotické 80S ribozómy sú umiestnené v cytoplazme, každý pozostáva z malej (40S) a veľkej (60S) podjednotky. 40S podjednotka pozostáva z 18S RNA (1900 nukleotidov) a 33 proteínov.[19][20] Veľká podjednotka sa skladá z 5S RNA (120 nukleotidov), 28S RNA (4700 nukleotidov), 5,8S RNA (160 nukleotidov) podjednotiek a 46 proteínov.[19][21][21]
| Ribozóm | Podjednotka | Molekuly rRNA | Ribozomálne proteíny |
|---|---|---|---|
| 80S | 60S | 28S (4718 nukleotidov) | 46 |
| 5,8S (160 nukleotidov) | |||
| 5S (120 nukloetidov) | |||
| 40S | 18S (1874 nukleotidov) | 33 |
Využitie rozdielov
[upraviť | upraviť zdroj]Rozdiely medzi bakteriálnymi a eukaryotickými ribozómami sa využívajú vo farmaceutickom priemysle na produkciu antibiotík, ktoré dokážu zničiť bakteriálnu infekciu bez poškodenia buniek infikovanej osoby. Kvôli rozdielom v štruktúre sú bakteriálne ribozómy 70S citlivé na antibiotiká, zatiaľ čo eukaryotické ribozómy 80S nie sú.[22] Aj keď mitochondrie majú ribozómy podobné tým bakteriálnym, antibiotiká ich neovplyvňujú, pretože mitochondrie sú obklopené dvojitou membránou, ktorá zabraňuje vstupu antibiotík dovnútra mitochondrie.[23]
Polyzómy
[upraviť | upraviť zdroj]U prokaryotov aj eukaryotov sa na jednej mRNA obvykle nachádza niekoľko ribozómov, čím sa syntéza proteínov značne urýchľuje. Hneď, ako sa ribozóm posunie po mRNA natoľko, že celkom uvoľní väzobné miesto, na toto miesto sa naviaže ďalší ribozóm. Jednotlivé ribozómy sú na mRNA vzdialené od seba približne 80 báz. Ribozómy pokračujú v syntéze proteínu až kým mRNA nie je degradovaná, čo sa stáva po niekoľkých minútach (prokaryotická mRNA) až po viac ako 10 hodinách (eukaryotické mRNA pre proteíny potrebné vo veľkých množstvách).[8]
Iné projekty
[upraviť | upraviť zdroj] Commons ponúka multimediálne súbory na tému Ribozóm
Commons ponúka multimediálne súbory na tému Ribozóm
Referencie
[upraviť | upraviť zdroj]Tento článok je čiastočný alebo úplný preklad článku Ribozom na českej Wikipédii.
- ↑ a b c d e f g h i j ROZSYPAL, Stanislav. Úvod do molekulární biologie. Zväzok 1. Brno : [s.n.], 1998. 3 zv. (česky)
- ↑ a b c d MIŠÚROVÁ, Eva; SOLÁR, Peter. Molekulová biológia. [s.l.] : Univerzita Pavla Jozefa Šafárika v Košiciach, 2007. ISBN 978-80-7097-671-5.
- ↑ a b c d e ŠKÁRKA, Bohumil; FERENČÍK, Miroslav. Biochémia. Bratislava : Alfa/Vydavateľstvo technickej a ekonomickej literatúry, 1983. Kapitola 8.2. Ribozómy, s. 225.
- ↑ PALADE, G. E.. A SMALL PARTICULATE COMPONENT OF THE CYTOPLASM. The Journal of Cell Biology, 1955-01-25, roč. 1, čís. 1, s. 59–68. Dostupné online [cit. 2019-08-24]. ISSN 0021-9525. DOI: 10.1083/jcb.1.1.59.
- ↑ ROBERTS, Richard B.. Microsomal particles and protein synthesis; papers presented at the First Symposium of the Biophysical Society, at the Massachusetts Institute of Technology, Cambridge, February 5, 6, and 8, 1958. Richard B. Roberts, editor.. New York, : Published on behalf of the Washington Academy of Sciences, Washington, D.C., by Pergamon Press,, 1958. Dostupné online.
- ↑ The Nobel Prize in Physiology or Medicine 1974 [online]. NobelPrize.org, [cit. 2019-08-24]. Dostupné online. (po anglicky)
- ↑ The Nobel Prize in Chemistry 2009 [online]. NobelPrize.org, [cit. 2019-08-24]. Dostupné online. (po anglicky)
- ↑ a b c d e f ALBERTS, Bruce; BRAY, Dennis; JOHNSON, Alexander, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter Základy buněčné biologie. Redakcia Miranda Brownová, Eleanor Lawrenceová, Valerie Nealová, Anne Vinnicombeová; preklad Arnošt Kotyk, Bohumil Bouzek, Pavel Hozák; ilustrácie Nigel Orme. 2. vyd. Ústí nad Labem : Espero Publishing, © 1998. ISBN 80-902906-2-0. Kapitola Od DNA k proteinu, s. 223 – 232. (česky)
- ↑ BRESLER, S. J.. Molekulární biologie. Preklad Stanislav Zadražil. Praha : ACADEMIA, 1979. (česky)
- ↑ Bruce Alberts et al. Essential Cell Biology. New York : Garland Science, 2004.
- ↑ a b c d e Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter. Molecular Biology of the Cell, 4rd edition [online]. . Dostupné online.
- ↑ MANGIAROTTI G., SCHESSINGER D.: J. mol. Biol. 20, 123 (1965)
- ↑ KAEMPFERVR., MESELSON M.: J. Mol. Biol. 31,277 (1968)
- ↑ KURLAND, C.G.. Molecular characterization of ribonucleic acid from Escherichia coli ribosomes. Journal of Molecular Biology, 1960-06, roč. 2, čís. 2, s. 83–91. Dostupné online [cit. 2019-08-24]. ISSN 0022-2836. DOI: 10.1016/s0022-2836(60)80029-0.
- ↑ NISSEN, P.. The Structural Basis of Ribosome Activity in Peptide Bond Synthesis. Science, 2000-08-11, roč. 289, čís. 5481, s. 920–930. Dostupné online [cit. 2019-08-24]. ISSN 0036-8075. DOI: 10.1126/science.289.5481.920.
- ↑ COLLATZ, E.; KÜCHLER, E.; STÖFFLER, G.. The site of reaction on ribosomal protein L27 with an affinity label derivative of tRNAmetf. FEBS Letters, 1976-04-01, roč. 63, čís. 2, s. 283–286. Dostupné online [cit. 2019-08-24]. ISSN 0014-5793. DOI: 10.1016/0014-5793(76)80112-3.
- ↑ CZERNILOFSKY, A. P.; COLLATZ, E. E.; STOFFLER, G.. Proteins at the tRNA Binding Sites of Escherichia coli Ribosomes. Proceedings of the National Academy of Sciences, 1974-01-01, roč. 71, čís. 1, s. 230–234. Dostupné online [cit. 2019-08-24]. ISSN 0027-8424. DOI: 10.1073/pnas.71.1.230.
- ↑ CZERNILOFSKY, A.P.; KURLAND, C.G.; STÖFFLER, G.. 30S Ribosomal proteins associated with the 3′-terminus of 16S RNA. FEBS Letters, 1975-10-15, roč. 58, čís. 1-2, s. 281–284. Dostupné online [cit. 2019-08-24]. ISSN 0014-5793. DOI: 10.1016/0014-5793(75)80279-1.
- ↑ a b BEN-SHEM, A.; GARREAU DE LOUBRESSE, N.; MELNIKOV, S.. The structure of the eukaryotic ribosome at 3.0 A resolution. This entry contains proteins of the 40S subunit, ribosome B [online]. dx.doi.org, 2011-12-21, [cit. 2019-08-24]. Dostupné online.
- ↑ RABL, J.; LEIBUNDGUT, M.; ATAIDE, S. F.. Crystal Structure of the Eukaryotic 40S Ribosomal Subunit in Complex with Initiation Factor 1. Science, 2010-12-23, roč. 331, čís. 6018, s. 730–736. Dostupné online [cit. 2019-08-24]. ISSN 0036-8075. DOI: 10.1126/science.1198308.
- ↑ a b KLINGE, S.; VOIGTS-HOFFMANN, F.; LEIBUNDGUT, M.. Crystal Structure of the Eukaryotic 60S Ribosomal Subunit in Complex with Initiation Factor 6. Science, 2011-11-03, roč. 334, čís. 6058, s. 941–948. Dostupné online [cit. 2019-08-24]. ISSN 0036-8075. DOI: 10.1126/science.1211204.
- ↑ RECHT, M. I.. Basis for prokaryotic specificity of action of aminoglycoside antibiotics. The EMBO Journal, 1999-06-01, roč. 18, čís. 11, s. 3133–3138. Dostupné online [cit. 2019-08-24]. ISSN 1460-2075. DOI: 10.1093/emboj/18.11.3133.
- ↑ O'BRIEN, T. W.. The general occurrence of 55 S ribosomes in mammalian liver mitochondria. The Journal of Biological Chemistry, 1971-05-25, roč. 246, čís. 10, s. 3409–3417. PMID 4930061. Dostupné online [cit. 2019-08-24]. ISSN 0021-9258.
Externé odkazy
[upraviť | upraviť zdroj]- FILIT – zdroj, z ktorého pôvodne čerpal tento článok.
