Kyselina oxaloctová
| Kyselina oxaloctová | |
 | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C4H4O5 |
| Synonymá | kyselina 2-oxobutándiová, 2-oxosukcinát, 2-ketosukcinát |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 132,07 g/mol |
| Teplota topenia | 161 °C |
| Termochemické vlastnosti | |
| Štandardná zlučovacia entalpia | -943,21 kJ/mol |
| Ďalšie informácie | |
| Číslo CAS | 328-42-7 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Kyselina oxaloctová[1] (známa aj ako OAA, z anglického oxaloacetic acid) je kryštalická organická zlúčenina, ktorej vzorec je HO2CC(O)CH2CO2H. Konjugovaná báza kyseliny oxaloctovej, nazývaná oxalacetát alebo oxaloctan, je metabolickým medziproduktom v mnohých procesoch u živočíchov a rastlín. Účastní sa glukoneogenézy, močovinového cyklu, glyoxylátového cyklu, syntézy aminokyselín, syntézy mastných kyselín a citrátového cyklu.[2]
Vlastnosti[upraviť | upraviť zdroj]
Kyselina oxaloctová je dikarboxylová ketokyselina. Postupne sa deprotonuje za vzniku dianiónu:
- HO2CC(O)CH2CO2H ⇌ −O2CC(O)CH2CO2H + H+, pKa = 2.22
- −O2CC(O)CH2CO2H ⇌ −O2CC(O)CH2CO2− + H+, pKa = 3.89
Pri vysokom pH sa ionizuje i enolizovateľný protón:
- −O2CC(O)CH2CO2− ⇌ −O2CC(O−)CHCO2− + H+, pKa = 13.03
Enol formy kyseliny oxaloctovej sú veľmi stabilné, dokonca má každý z nich iný bod topenia (152 °C pre cis izoformu a 184 °C pre trans izoformu). Reakcia je katalyzovaná oxalacetáttautomerázou. trans-enol-oxalacetát vzniká i pôsobením fumarázy na kyselinu vínnu.[3]

Biosyntéza[upraviť | upraviť zdroj]
Oxalacetát sa v prírode vytvára niekoľkými spôsobmi. Hlavným spôsobom je oxidácia L-malátu, ktorá je katalyzovaná malátdehydrogenázou v citrátovom cykle. Malát sa takisto oxiduje sukcinátdehydrogenázou za vzniku enol-oxalacetátu, reakcia je však pomalá.[4]
Takisto vzniká kondenzáciou pyruvátu s kyselinou uhličitou poháňanou hydrolýzou ATP:
- CH3C(O)CO2− + HCO3− + ATP → −O2CCH2C(O)CO2− + ADP + Pi
Táto reakcia prebieha v listovom mezofyle rastlín. Jej medziproduktom je fosfoenolpyruvát a katalyzuje ju fosfoenolpyruvátkarboxyláza.
Oxalacetát môže vznikať i transamináciou či deamináciou kyseliny asparágovej.
Biochemický význam[upraviť | upraviť zdroj]
Oxalacetát je intermediátom v citrátovom cykyle, kde reaguje s acetylkoenzýmom A za vzniku citrátu (kyseliny citrónovej). Reakciu katalyzuje citrátsyntáza. Takisto sa nachádza v glukoneogenéze, glyoxylátovom cykle, syntézy aminokyselín a syntézy mastných kyselín. Oxalacetát je silný inhibítor komplexu II (sukcinátdehydrogenázy).
Glukoneogenéza[upraviť | upraviť zdroj]
Glukoneogenéza[2] je metabolická dráha, ktorej výsledkom je glukóza syntetizovaná z látok iných, než sacharidov. Začiatok tohto procesu prebieha v mitochondriálnej matrix, kde sa nachádzajú molekuly pyruvátu. Pyruvát je karboxylovaný pomocou pyruvátkarboxylázy aktivovanej molekulami ATP a vodou. V tejto reakci vyzniká oxalacetát. Ten je následne redukovaný pomocou NADH za vzniku malátu. Vďaka tejto zmene je možný transport molekuly mimo mitochondrie. Až je malát v cytosóle, oxiduje sa naspäť na oxalacetát pomocou NAD+. Oxalacetát ostáva v cytosóle, kde následne prebehne zvyšok reakcií glukoneogenézy. Oxalacetát je dekarboxylovaný a fosforylovaný pomocou fosfoenolpyruvátkarboxykinázy, pričom z neho vzniká 2-fosfoenolpyruvát. Zdrojom fosfátu je GTP (guanozíntrifosfát). Ďalším sledom reakcií, väčšinou zhodných s glykolýzou (ale v opačnom smere) sa získa glukóza.
Močovinový cyklus[upraviť | upraviť zdroj]
Močovinový cyklus je metabolická dráha, ktorá vedie k tvorbe močoviny z dvoch molekúl amoniaku a jednej molekuly uhličitanu.[2] Tento proces bežne prebieha v hepatocytoch (bunkách pečene). Reakcie súvisiace s močovinovým cyklom produkujú NADH, ktorý je možné vyprodukovať dvomi spôsobmi. Jeden z nich využíva oxalacetát. V cytosóle sú prítomné molekuly fumarátu, ktorý je možné premeniť na malát pomocou fumarázy. Malát sa následne premení na oxalacetát pomocou malátdehydrogenázy, pričom vzniká NADH. Vzniknutý oxalacetát sa recykluje a vzniká aspartát, keďže transaminázy preferujú ketokyseliny ako svoj strubstrát. Tým je zároveň zariadený prívod dusíku do bunky. Aspartát sa takisto účastní močovinového cyklu.

Glyoxylátový cyklus[upraviť | upraviť zdroj]
Glyoxylátový cyklus je variant citrátového cyklu.[5] Je to anabolická dráha prebiehajúca v rastlinách a baktériách využívajúca enzýmy izocitrátlyáza a malátsyntáza. Niektoré medzikroky cyklu sú odlišné oproti citrátovému cyklu, oxalacetát má však v oboch cykloch rovnakú funkciu.[2] Oxalacetát teda reaguje ako prvý reaktant a vzniká ako posledný produkt i v glyoxylátovom cykle. Celkovým ziskom v glyoxylátovom cykle je vlastne jedna molekula oxalacetátu, pretože do cyklu vstupujú dve molekuly acetylkoenzýmu A.
Syntéza mastných kyselín[upraviť | upraviť zdroj]
Počas syntézy mastných kyselín je acetylkoenzým A presunutý z mitochondrie do cytoplazmy, kde sa nachádza enzým syntáza mastných kyselín. Acetylkoenzým A je transportovaný z matrixu mitochondrie v podobe citrátu, ktorý vzniká reakciou acetylkoenzýmu A s oxalacetátom. Táto reakcia je zvyčajne prvou reakciou citrátového cyklu, ale ak nie je nutný zisk energie, tak sa citrát presúva do cytoplazmy, kde sa opäť rozkladá na acetylkoenzým A a oxalacetát. Vďaka tomu môže začať syntéza mastných kyselín.
Iná časť cyklu využíva NADPH na syntézu mastných kyselín.[6] Časť tohto redukčného činidla sa získava pri presune oxalacetátu z cytosólu do mitochondrie, pričom vnútorná vrstva mitochondrie nesmie byť pre oxalacetát priepustná. Oxalacetát sa najprv redukuje na malát pomocou NADH a malát sa potom dekarboxyluje na pyruvát. Pyruvát môže prejsť do mitochondrie, kde sa opäť karboxyluje (za účasti uhličitanu) na oxalacetát pomocou pyruvátkarboxylázy.
Týmto spôsobom je počas presunu acetylkoenzýmu A z mitochondrie do cytoplazmy produkovaná molekula NADH. Celkovou reakciou, ktorá je spontánna, je teda:
- HCO3– + ATP + acetyl-CoA → ADP + Pi + malonyl-CoA
Syntéza aminokyselín[upraviť | upraviť zdroj]
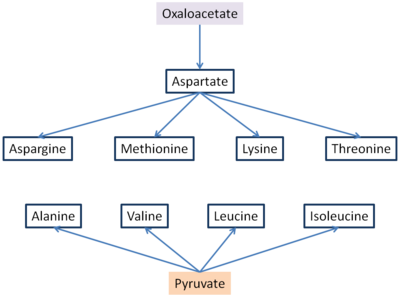
Štyri esenciálne aminokyseliny a dve neesenciálne aminokyseliny sú syntetizované z oxalacetátu.[7] Z oxalacetátu sa transamináciou tvorí aspartát pomocou aspartátaminotransferázy. Z aspartátu sú následne syntetizované asparagín, metionín, lyzín a treonín. Z treonínu sa ďalej syntetizuje izoleucín. Bez oxalacetátu by teda syntéza týchto aminokyselín vôbec nemohla prebehnúť, keďže sa z neho syntetizuje aspartát.
Biosyntéza oxalátu[upraviť | upraviť zdroj]
Z oxalacetátu sa hydrolýzou tvorí oxalát (šťaveľan):[8]
- oxalacetát + H2O ⇌ oxalát + acetát
Tento proces je katalyzovaný oxalacetázou. Tento enzým sa nachádza v rastlinách, ale u živočíchov vôbec nie je známy.[9]
Referencie[upraviť | upraviť zdroj]
- ↑ ŠKÁRKA, Bohumil; FERENČÍK, Miroslav. Biochémia. 3. vyd. [s.l.] : [s.n.], 1992. ISBN 80-05-01076-1. S. 156, 163.
- ↑ a b c d NELSON, David L.; COX, Michael M.. Principles of Biochemistry. 4th. vyd. New York : W. H. Freeman, 2005. ISBN 0-7167-4339-6.
- ↑ VAN VUGT-LUSSENBURG, Barbara M. A.; VAN DER WEEL, Laura; HAGEN, Wilfred R.. Biochemical Similarities and Differences between the Catalytic [4Fe-4S] Cluster Containing Fumarases FumA and FumB from Escherichia coli. PLoS ONE, 2013-02-06, roč. 8, čís. 2, s. e55549. Dostupné online [cit. 2021-02-27]. ISSN 1932-6203. DOI: 10.1371/journal.pone.0055549. (po anglicky)
- ↑ Direct demonstration of enol-oxaloacetate as an immediate product of malate oxidation by the mammalian succinate dehydrogenase. FEBS Letters, 1991, s. 76–78. DOI: 10.1016/0014-5793(91)80944-X.
- ↑ Welcome to The Chemistry Place [online]. . Dostupné online.
- ↑ fatty acids synthesis. http://www.rpi.edu/dept/bcbp/molbiochem/MBWeb/mb2/part1/fasynthesis.htm.
- ↑ http://faculty.ksu.edu.sa/69436/Documents/lecture-15-aa_from_oxaloacetate_and_pyruvate.pptx [online]. . Dostupné online. Archivované 2013-10-21 z originálu.
- ↑ Gadd, Geoffrey M. "Fungal production of citric and oxalic acid: importance in metal speciation, physiology and biogeochemical processes" Advances in Microbial Physiology (1999), 41, 47-92.
- ↑ Xu, Hua-Wei. "Oxalate accumulation and regulations is independent of glycolate oxidase in rice leaves" Journal of Experimental Botany, Vol 57, No. 9 pp. 1899-1908, 2006
Zdroj[upraviť | upraviť zdroj]
Tento článok je čiastočný alebo úplný preklad článku Oxaloacetic acid na anglickej Wikipédii.
