Pentóza
Pentóza je monosacharid s piatimi atómami uhlíka, so sumárnym vzorcom C5H10O5. Majú molárnu hmotnost 150,13 g/mol. Názov pentóza je odvodený od gréckej číslovky päť (penta) a charakteristickej prípony pre sacharidy -óza. Podľa prítomnosti karbonylovej skupiny rozoznávame ketopentózu (obsahuje ketónovú funkčnú skupinu, zväčša na druhom alebo treťom uhlíku) a aldopentózu (obsahuje aldehydickú funkčnú skupinu, na prvom uhlíku). Na všetkých ostatných uhlíkoch majú hydroxylovú skupinu. Podobne ako iné monosacharidy, pentózy sa vyskytujú ako lineárne alebo cyklické molekuly. Tieto formy sa vo vodných roztokoch ľahko menia jedna na druhú.[1] Lineárna forma zvyčajne existuje len v roztoku.
Pod pentózy sa občas zaradzujú i deoxypentózy, ktoré vznikajú z pentóz odobratím jedného alebo viacerých atómov kyslíka. Ich všeobecný vzorec je C5H10O5-y, kde y je počet odobratých kyslíkov.
Pentózy sú veľmi dôležité hlavne v biochémii. Ribóza je zložkou RNA a jej príbuzná deoxyribóza je zložkou DNA. Fosforylované pentózy sú dôležitými produktami sú pentózafosfátovej dráhy, a to hlavne ribóza-5-fosfát (R5P), ktorá sa využíva na syntézu nukleotidov a nukleových kyselín. D-Ribulóza slúži ako akceptor oxidu uhličitého pri fotosyntéze.
Aldopentóza
[upraviť | upraviť zdroj]Aldopentózy majú tri centrá chirality a preto je možných osem rozličných stereoizomérov. Podľa vzájomnej pozície hydroxylových skupín sa označujú "D" alebo "L" (nezávisle na ich optickej aktivite). Z týchto sa v prírode nachádza len D-ribóza, D-xylóza, D-arabinóza a L-arabinóza. Lyxóza sa v prírode nevyskytuje v čistej forme.
 D-Arabinóza |
 D-Lyxóza |
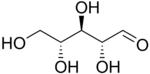 D-Ribóza |
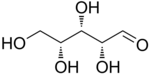 D-Xylóza |
 L-Arabinóza |
 L-Lyxóza |
 L-Ribóza |
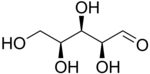 L-Xylóza |
Ketopentóza
[upraviť | upraviť zdroj]Ketopentózy majú dva stredy chirality, preto sú možné štyri stereoizoméry. V prírode sa z týchto vyskytujú iba D-izoméry. Ketopentózy, ktoré majú karbonylovú skupinu na 3. uhlíku sú vzácne.
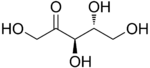 D-Ribulóza |
 D-Xylulóza |
 L-Ribulóza |
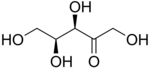 L-Xylulóza |
Cyklická forma
[upraviť | upraviť zdroj]
Cyklická forma pentóz vzniká interakciou karbonylovej skupiny s hydroxylovou skupinou na inom uhlíku, čím sa z hydroxylu stáva éterový mostík mezdi dvoma uhlíkmi. Touto intramolekulárnou reakciou vznikajú cyklické zlúčeniny, ktoré sú všeobecne označené ako furanózy, pretože pripomínajú molekulu tetrahydrofuránu.[1] Kvôli vzniku kruhu sa karbonylový uhlík stáva chirálnym centrom, ktoré môže mať dve konfigurácie podľa polohy hydroxylovej skupiny. Každá lineárna forma pentózy môže teda vytvoriť dve cyklické formy, nazývané anoméry, ktoré sa označujú α a β.
Deoxypentózy
[upraviť | upraviť zdroj]Dôležitou deoxypentózou je 2-deoxyribóza, ktorá má dva izoméry.
 D-Deoxyribóza D-Deoxyribóza
|
 L-Deoxyribóza L-Deoxyribóza
|
Vlastnosti
[upraviť | upraviť zdroj]V bunke majú pentózy vyššiu metabolickú stabilitu než hexózy.
Polyméry zložené z pentóz sa nazávajú pentozany.
Skúšky na pentózy
[upraviť | upraviť zdroj]
Najdôležitejšie skúšky na pentózy využíva premenu pentóz na furfural, ktorý následne reaguje s chromofórom. U Tollensovej skúšky na pentózy (odlišnej od Tollensovej skúšky so strieborným zrkadielkom, používaného pre zistenie prítomnosti redukujúcich cukrov) reaguje furfural s floroglucinolom, čím vzniká farebná zlúčenina.[2] U anilínacetátového testu reaguje furfural s anilínacetátom[3] a u Bialovho testu s orcinolom.[4] V každom z týchto testov reagujú pentózy silnejšie a rýchlejšie než hexózy.
Referencie
[upraviť | upraviť zdroj]- ↑ a b Morrison, Robert Thornton; Boyd, Robert Neilson. Organic Chemistry. 2nd. vyd. [s.l.] : Allyn and Bacon. Library of Congress catalog 66-25695
- ↑ Oshitna, K., and Tollens, B., Ueber Spectral-reactionen des Methylfurfurols. Ber. Dtsch. Chem. Ges. 34, 1425 (1901)
- ↑ SEAGER, Spencer L.; SLABAUGH, Michael R.; HANSEN, Maren S.. Safety Scale Laboratory Experiments. [s.l.] : Cengage Learning, 2016-12-05. Dostupné online. ISBN 9781337517140. S. 358. (po anglicky)
- ↑ PAVIA, Donald L.. Introduction to Organic Laboratory Techniques: A Small Scale Approach. [s.l.] : Cengage Learning, 2005. Dostupné online. ISBN 0534408338. S. 447. (po anglicky)
Zdroj
[upraviť | upraviť zdroj]Tento článok je čiastočný alebo úplný preklad článku Pentosen na nemeckej Wikipédii. Tento článok je čiastočný alebo úplný preklad článku Pentose na anglickej Wikipédii.
