Metylmalonylkoenzým A
| Metylmalonylkoenzým A | |
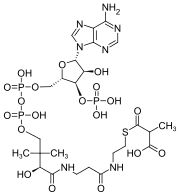 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C25H40N7O19P3S |
| Synonymá | Metylmalonyl-CoA |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 867,608 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 1264-45-5 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Metylmalonylkoenzým A alebo metylmalonyl-CoA je tioester, ktorý sa skladá z koenzýmu A naviazaného na kyselinu metylmalónovú. Je to dôležitý intermediát v syntéze sukcinyl-CoA, ktorý má dôležitú úlohu v citrátovom cykle.[1][2] Niekedy sa táto zlúčenina označuje i ako metylmalyl-CoA.[3]
Metylmalonyl-CoA je na rozdiel od kyseliny metylmalónovej chirálna zlúčenina, ktorá sa v tele vyskytuje v oboch izoméroch (ako (R) i (S)). Oba izoméry vystupujú v jeho metabolizme.[4]
Biosyntéza a metabolizmus[upraviť | upraviť zdroj]
Metylmalonyl-CoA vzniká v metabolizme mastných kyselín s nepárnym počtom atómov uhlíka[2] alebo z bočných reťazcov cholesterolu, kde vzniká propionyl-CoA.[5] Propionyl-CoA takisto vzniká v metabolizme niektorých aminokyselín (konkrétne Met, Ile a Val) a i pri rozklade tymínu.[4]
Reakcie[upraviť | upraviť zdroj]
Propionyl-CoA sa spolu s hydrogenuhličitanom premieňajú na metylmalonyl-CoA v reakcii katalyzovanej enzýmom propionyl-CoA karboxylázou:[1][4]
- propionyl-CoA + HCO3- → (S)-metylmalonyl-CoA
V procese však vzniká (S)-izomér, ktorý potom metylmalonyl-CoA racemáza premieňa na (R)-izomér:[4]
- (S)-metylmalonyl-CoA ↔ (R)-metylmalonyl-CoA
(R)-Metylmalonyl-CoA sa potom premieňa na sukcinyl-CoA pomocou metylmalonyl-CoA mutázy:[4]
- (R)-metylmalonyl-CoA → sukcinyl-CoA
Táto reakcia je reverzibilná izomerizácia. Jej produktom je sukcinyl-CoA, ktorý vstupuje do citrátového cyklu. Ide teda o anaplerotickú reakciu. Alternatívne sa môže sukcinyl-CoA premeniť na malát a následne na pyruvát a acetyl-CoA, čo umožňuje jeho rozloženie a zisk energie.[4]
Biosyntéza mastných kyselín a polyketidov[upraviť | upraviť zdroj]
Metylmalonyl-CoA sa okrem premeny na sukcinyl-CoA môže účastniť i biosyntézy zložitejších organických zlúčenín. Syntáza mastných kyselín ho môže občasne zabudovať do mastných kyselín, čím dochádza k vzniku vetvených mastných kyselín.[6] Okrem toho sa metylmalonyl-CoA účastní biosyntézy polyketidov, ktorá prebieha u baktérií, rastlín, húb a niektorých živočíšnych vývojových vetví. Polyketidsyntázy (PKS) sú schopné do reťazca zabudovať (2S)-metylmalonyl-CoA a tým budovať vetvené polyketidy, z ktorých sa syntetizuje napríklad erytromycín, ktorý pôsobí ako antibiotikum, alebo aureotín, ktorý má antifungálne účinky a pôsobí proti rakovine.[7]
Vitamín B12[upraviť | upraviť zdroj]
Vitamín B12 má dôležitú úlohu pri premene metylmalonyl-CoA. Adenozylkobalamín (jedna z foriem vitamínu B12) je organokovová zlúčenina, ktorá sa účastní reakcie metylmalonyl-CoA mutázy, čo je enzým nutný pre ľudské telo.[8] Reakcia, ktorú tento enzým katalyzuje, je radikálová reakcia.[8]
Patológia[upraviť | upraviť zdroj]
Metylmalónová acidémia (MMA)[upraviť | upraviť zdroj]
Táto porucha vzniká, keď metylmalonyl-CoA mutáza nie je schopná izomerizovať dostatočné množstvo metylmalonyl-CoA na sukcinyl-CoA.[9] Na základe toho vzniká nadbytok kyseliny propiónovej a/alebo kyseliny metylmalónovej, čo u dojčiat spôsobuje závažné poškodenie mozgu až smrť.[10] Táto porucha je spojená i s vitamínom B12, ktorý pôsobí ako kofaktor v reakcii katalyzovanej metylmalonyl-CoA mutázou.[9][11]
Kombinovaná malónová a metylmalónová acidúria (CMAMMA)[upraviť | upraviť zdroj]
Pri metabolickom ochorení kombinovanej malónovej a metylmalónovej acidúrie (CMAMMA) spôsobenom ACSF3 je znížená expresia metylmalonyl-CoA syntetáza, ktorá premieňa toxickú kyselinu metylmalónovú na metylmalonyl-CoA, a tak ju dodáva do citrátového cyklu.[12][13] Výsledkom je akumulácia kyseliny metylmalónovej.
Referencie[upraviť | upraviť zdroj]
- ↑ a b Propionyl-CoA carboxylase - A review. Molecular Genetics and Metabolism, December 2017, s. 145–152. DOI: 10.1016/j.ymgme.2017.10.002. PMID 29033250.
- ↑ a b ŠKÁRKA, Bohumil; FERENČÍK, Miroslav. Biochémia. 3. vyd. [s.l.] : [s.n.], 1992. ISBN 80-05-01076-1. S. 228-230.
- ↑ LEHNINGER, Albert L.. Lehninger principles of biochemistry. New York : W.H. Freeman, 2005. (Fourth edition.) Dostupné online. ISBN 0-7167-4339-6.
- ↑ a b c d e f VOET, Donald. Biochemistry. Hoboken, NJ : John Wiley & Sons, 2011. (4th edition.) Dostupné online. ISBN 978-0-470-57095-1. S. 952-957, 1136.
- ↑ Proposed guidelines for the diagnosis and management of methylmalonic and propionic acidemia. Orphanet Journal of Rare Diseases, September 2014, s. 130. DOI: 10.1186/s13023-014-0130-8. PMID 25205257.
- ↑ DEWULF, Joseph P.; GERIN, Isabelle; RIDER, Mark H.. The synthesis of branched-chain fatty acids is limited by enzymatic decarboxylation of ethyl- and methylmalonyl-CoA. Biochemical Journal, 2019-08-30, roč. 476, čís. 16, s. 2427–2447. PMID: 31416829 PMCID: PMC6717113. Dostupné online [cit. 2023-10-29]. ISSN 0264-6021. DOI: 10.1042/BCJ20190500.
- ↑ CHAN, Yolande A.; PODEVELS, Angela M.; KEVANY, Brian M.. Biosynthesis of Polyketide Synthase Extender Units. Natural product reports, 2009-01, roč. 26, čís. 1, s. 90. PMID: 19374124. Dostupné online [cit. 2023-10-29]. DOI: 10.1039/b801658p. (po anglicky)
- ↑ a b Biochemistry of B12-Cofactors in Human Metabolism. Dordrecht : Springer Netherlands, 2012. ISBN 978-94-007-2198-2. DOI:10.1007/978-94-007-2199-9_17 S. 323–346.
- ↑ a b Role of vitamin B12 on methylmalonyl-CoA mutase activity. Journal of Zhejiang University. Science. B, June 2012, s. 423–437. DOI: 10.1631/jzus.B1100329. PMID 22661206.
- ↑ BAUMGARTNER, Matthias R.; HÖRSTER, Friederike; DIONISI-VICI, Carlo. Proposed guidelines for the diagnosis and management of methylmalonic and propionic acidemia. Orphanet Journal of Rare Diseases, 2014-09-02, roč. 9, čís. 1, s. 130. Dostupné online [cit. 2022-10-29]. ISSN 1750-1172. DOI: 10.1186/s13023-014-0130-8.
- ↑ TAKAHASHI-IÑIGUEZ, Tóshiko; GARCÍA-HERNANDEZ, Enrique; ARREGUÍN-ESPINOSA, Roberto. Role of vitamin B12 on methylmalonyl-CoA mutase activity. Journal of Zhejiang University SCIENCE B, 2012-06-01, roč. 13, čís. 6, s. 423–437. Dostupné online [cit. 2022-10-29]. ISSN 1862-1783. DOI: 10.1631/jzus.B1100329. (po anglicky)
- ↑ BOWMAN, Caitlyn E.; WOLFGANG, Michael J.. Role of the malonyl-CoA synthetase ACSF3 in mitochondrial metabolism. Advances in Biological Regulation, 2019-01, roč. 71, s. 34–40. Dostupné online. DOI: 10.1016/j.jbior.2018.09.002. (po anglicky)
- ↑ GABRIEL, Marie Cosette; RICE, Stephanie M.; SLOAN, Jennifer L.. Considerations of expanded carrier screening: Lessons learned from combined malonic and methylmalonic aciduria. Molecular Genetics & Genomic Medicine, 2021-04, roč. 9, čís. 4. Dostupné online. ISSN 2324-9269. DOI: 10.1002/mgg3.1621. (po anglicky)
Zdroj[upraviť | upraviť zdroj]
Tento článok je čiastočný alebo úplný preklad článku Methylmalonyl-CoA na anglickej Wikipédii.
