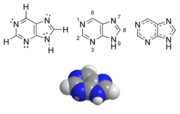
Purín
| Purín | |
 | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C5H4N4 |
| Synonymá | 9H-purín |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 120,11 g/mol |
| Teplota topenia | 214 °C |
| Ďalšie informácie | |
| Číslo CAS | 120-73-0 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Purín je aromatická heterocyklická organická zlúčenina zložená z pyrimidínového a imidazolového jadra. Puríny, vrátane substitouvaných purínov a tautomérov, patria k najbežnejším dusíkatým heterocyklom v prírode. Puríny a pyrimidíny vytvárajú 2 skupiny dusíkatých báz. Dve zo štyroch deoxyribonukleových báz a dve zo štyroch ribonukleových báz sú puríny. Sú to adenín a guanín.[1]
Dôležité puríny[upraviť | upraviť zdroj]
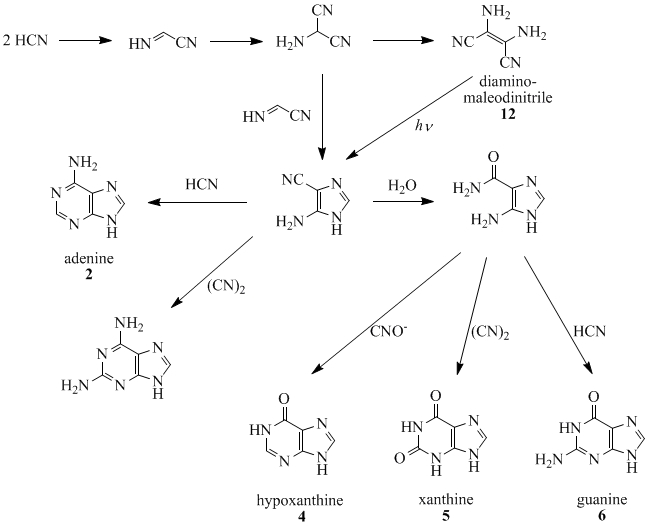
V prírode sa nachádza mnoho purínov. Dve dusíkaté bázy sú puríny adenín a guanín. Iné dôležité puríny sú hypoxantín, xantín, teobromín, kofeín, kyselina močová a izoguanín.
Funkcia[upraviť | upraviť zdroj]
Okrem hlavnej úlohy purínov pri stavbe DNA a RNA sú puríny tiež zložkou mnohých dôležitých biomolekúl, ako sú napríklad ATP, GTP, cyklický AMP, NADH alebo koenzým A. Purín samotný sa dosiaľ v prírode nenašiel, ale je ho možné laboratórne syntetizovať.
Puríny tiež môžu mať funkciu neurotransmiterov (látok schopných prenášať informáciu medzi neurónmi) pracujúcich na princípe purínergických receptorov. Adenozín aktivuje adenozínové receptory.
História[upraviť | upraviť zdroj]
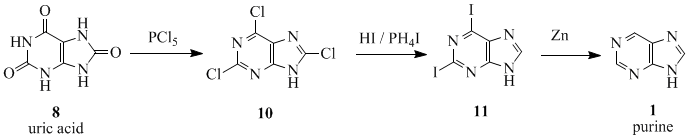
Pomenovanie "purín" (purum uricum) zaviedol nemecký chemik Emil Fischer v roku 1884. Dokázal ho poprvýkrát syntetizovať v roku 1899. Ako východiskovú látku použil kyselinu močovú, ktorá bola po prvý raz izolovaná z obličkových kameňov Scheeleom v roku 1776. Potom ju nechal zreagovať s chloridom fosforečným za vzniku 2,6,8-trichlóropurínu, ktorý bol následne premenený jodovodíkom a fosfónium jodidom na 2,6-dijódopurín. Potom následnej redukcii zinkovým práškom vznikol purín.[2][3]
Metabolizmus[upraviť | upraviť zdroj]
Mnoho organizmov má metabolické dráhy schopné syntetizovať alebo rozložiť puríny. Sú prírodne syntetizované ako nukleotidy. Až 90% purínov sa v rámci organizmu recykluje, pretože ich syntéza je energeticky veľmi náročná.
Zdroje purínov[upraviť | upraviť zdroj]
Puríny sa nachádzajú vo vysokých koncentráciách v mäse, v niektorých vnútorných orgánoch, v ančovičkách, v herringoch, makrelách alebo v pive. Vegetariánska strava je chudobná na puríny.[4][5]
Syntéza[upraviť | upraviť zdroj]
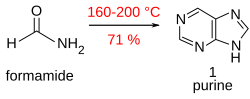
Okrem syntézy in vivo je možná aj umelá syntéza. Purín sa dá získať s dobrým výnosom (asi 71%) zahrievaním formamidu:
Táto pozoruhodná reakcia sa preberá v teórii o vzniku života na Zemi.
Ďalšia možná schéma: formamid sa zahreje v otvorenej nádobe zhruba na 28 hodín v olejovom kúpeli na 170-190 °C. Po oddestilovaní zvyšného formamidu sa urobí reflux metanolom. Nasleduje filtrácia, potom destilácia a produktom je takmer čistý purín.[6]
Zdroje[upraviť | upraviť zdroj]
- ↑ Rosemeyer, H. Chemistry & Biodiversity 2004, 1, 361.
- ↑ Fischer, E. Berichte der Deutschen Chemischen Gesellschaft 1899, 32, 2550.
- ↑ Scheele, V. Q. Examen Chemicum Calculi Urinari, Opuscula, 1776, 2, 73.
- ↑ Archivovaná kópia [online]. [Cit. 2012-06-15]. Dostupné online. Archivované 2011-11-12 z originálu.
- ↑ Gout Diet: Limit High Purine Foods
- ↑ Yamada, H.; Okamoto, T.. A One-step Synthesis of Purine Ring from Formamide. Chemical & Pharmaceutical Bulletin, 1972, s. 623. Dostupné online. DOI: 10.1248/cpb.20.623.